Dẫn khí Clo vào dung dịch chứa 44,8(g0 Natri hidroxit vừa đủ thu được Natri Clorua , Natri hipoclorit ( NaCLO) và Nước . Tính khối lượng Muối ăn thu được bằng 2 cách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)\(n_{Na}=\dfrac{m_{Na}}{M_{Na}}=\dfrac{2,76}{23}=0,12\left(mol\right)\)
\(PTHH:2Na+2H_2O\xrightarrow[]{}2NaOH+H_2\)
tỉ lệ : 2 2 2 1 (mol)
số mol : 0,12 0,12 0,12 0,06 (mol)
Giá trị của V là:
\(V_{H_2}=n_{H_2}.22,4=0,06.22,4=1,344\left(l\right)\)
b)Khối lượng của natri hiđroxit là:
\(m_{NaOH}=n_{NaOH}.M_{NaOH}=0,12.40=4,8\left(g\right)\)
Nồng độ phần trăm của dung dịch natri hiđroxi là:
\(C_{\%NaOH}=\dfrac{m_{NaOH}}{m_{dd}}.100\%=\dfrac{4,8}{200}.100\%=2,4\%\)
c) Thể tích của \(\dfrac{1}{2}\) lượng khí trên là:
\(V_{H_22}=\dfrac{V_{H_2}}{2}=\dfrac{1,344}{2}=0,672\left(l\right)\)
Số mol của \(\dfrac{1}{2}\) lượng khí trên là:
\(n_{H_22}=\dfrac{V_{H_2}}{22,4}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
\(PTHH:Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\)
tỉ lệ :1 2 1 1 (mol)
số mol :0,03 0,06 0,03 0,03 (mol)
Khối lượng sắt cần dùng để thu được \(\dfrac{1}{2}\) lượng khí trên là:
\(m_{Fe}=n_{Fe}.M_{Fe}=0,03.56=1,68\left(g\right)\)

a)
Khối lượng của dung dịch:
\(m_{dd}=m_{ct}+m_{dm}=20+180=200\left(g\right)\)
Nồng độ phần trăm của dung dịch:
\(C\%=\dfrac{m_{ct}}{m_{dd}}.100\%=\dfrac{20}{200}.100\%=10\%\)
b) đề sai nha bạn

Câu 1:
\(2Na+Br_2\rightarrow2NaBr\\ n_{NaBr}=\dfrac{61,8}{103}=0,6\left(mol\right)\\ n_{Na}=n_{NaBr}=0,6\left(mol\right)\\ n_{Br_2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ \Rightarrow a=m_{Na}=0,6.23=13,8\left(g\right)\\ m_{Br_2}=0,3.160=48\left(g\right)\\ m_{ddBr_2}=\dfrac{48}{5\%}=960\left(g\right)\)
Câu 2:
\(2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ n_{FeCl_3}=\dfrac{40,625}{162,5}=0,25\left(mol\right)\\ n_{Fe}=n_{FeCl_3}=0,25\left(mol\right)\\ \Rightarrow m=m_{Fe}=0,25.56=14\left(g\right)\\ n_{Cl_2}=\dfrac{3}{2}.0,25=0,375\left(mol\right)\\ V_{Cl_2\left(đktc\right)}=0,375.22,4=8,4\left(l\right)\)

Bảo toàn KL: \(m_{Na_2SO_4}+m_{CaCl_2}=m_{NaCl}+m_{CaSO_4}\)
\(\Rightarrow m_{CaSO_4}=14,2+11,1-17=8,3\left(g\right)\)

Bài 1:
Na2O + H2O → 2NaOH
Bài 2:
a) 2Fe + 3Cl2 → 2FeCl3
b) Áp dụng định luật bảo toàn khối lượng ta có:
\(m_{Fe}+m_{Cl_2}=m_{FeCl_3}\)
\(\Rightarrow m_{FeCl_3}=11,2+21,3=32,5\left(g\right)\)


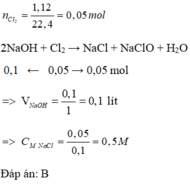

Cl2 + 2NaOH → NaCl + NaClO + H2O
nNaOH = \(\dfrac{44,8}{40}\)= 1,12 mol.
=> nNaCl = \(\dfrac{1,12}{2}\)= 0,56 <=> mNaCl = 0,56.58,5 = 32,76 gam
Cách 2: Áp dụng ĐLBT khối lượng => mNaCl = mCl2 + mNaOH - mNaClO- mH2 = 0,56.71 + 1,12.40 - 0,56. 74,5 - 0,56.18 = 32,76 gam