Hấp thụ hoàn toàn 3,36 lít CO2(đktc) vào 100ml dung dịch gồm Na2CO3 0,25M và KOH a mol/l , sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y . Cho toàn bộ Y tác dụng với dung dịch Ca(NO3)2 , thu được 7,5 gam kết tủa . Giá trị của a là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : A
nCO2 = 0,15 mol ; nCaCO3 = 0,075 mol
Bảo toàn C : nHCO3 = nCO2 + nNa2CO3 – nCaCO3 = 0,1 mol
=> Trong Y có : 0,05 mol Na+ ; 0,1a mol K+ ; 0,075 mol CO32- ; 0,1 mol HCO3-
Bảo toàn điện tích : 0,05 + 0,1a = 0,075.2 + 0,1
=> a = 2

Đáp án A
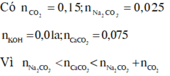
Nên khi hấp thụ CO2 vào dung dịch ban đầu thì CO2 phản ứng với OH- tạo
H C O 3 - , C O 3 2 -
Khi đó trong dung dịch Y có 0,025 mol Na2CO3, a mol K2CO3 và b mol KHCO3
Nên
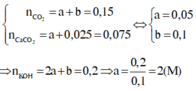

Đáp án B
![]()
Như vậy, khi CO2 phản ứng với KOH đã tạo ra thêm 0,03 mol CO3 2-
Do hấp thụ hoàn toàn nên lượng HCO3- tạo ra là 0,12 mol![]()
=>Đáp án B

![]()
Cho toàn bộ Y tác dụng với dung dịch BaCl2 dư được 11,82 gam kết tủa, đó là BaCO3.
Ta có: 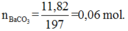
Ta đặt: số mol KOH là: nKOH = 0,1x mol, dd Y chứa KHCO3 = y mol
Nhận thấy ở đây, nếu ta dùng bảo toàn các nguyên tố trước và sau phản ứng thì ta sẽ có các mối liên hệ giữa x và y:
Bảo toàn nguyên tố C ta có:
![]()
Hay 0,1 + 0,02 = 0,06 +y ⇒ y = 0,06 mol
• Bảo toàn nguyên tố K ta được:
![]()
hay 2.0,22+0,1x = 2.0.06+y => x = 1,4
Đáp án B

Đáp án : B
Ta có :
n CO2 = 0,1 mol ; n BaCO3 = 11,82 / 197 = 0,06 mol
n K2CO3 = 0,02 mol
khi sục khí CO2 vào dung dịch hỗn hợp gồm K2CO3 và KOH
giả sử chỉ xảy ra phản ứng :
CO2 + 2KOH → K2CO3 + H2O
0,1 0,1
=> n K2CO3(Trong dd ) = 0,1 + 0,02 = 0,12 mol
BaCl2 + K2CO3 →BaCO3 ↓+ KCl
0,12 0,12
Ta thấy : n ↓ = 0,12 ≠ n ↓ đề cho = 0,06 mol
Vậy trong phản ứng CO2 với KOH ngoài muối K2CO3 còn có muối KHCO3.
Áp dụng định luật bảo toàn nguyên tố C ta có :
n C(trong CO2) + n C(trong K2CO3) = n C(trong BaCO3) + n C(trong KHCO3)
=> 0,1 + 0,02 = 0,06 + x (x là số mol BaCO3 )
=> x = 0,06
CO2 + KOH → KHCO3
0,06 0,06 0,06
CO2 + 2KOH → K2CO3 + H2O
0,04 0,08
=> nKOH = 0,14 mol
=> [ KOH ] = 0,14/ 0,1 = 1,4 M


