Thủy phân 132 gam một chất béo trung tính cần vừa đủ 18 gam NaOH. Đốt cháy 0,5 mol chất béo này sinh ra 28,5 mol CO2. Tính khối lượng H2 để chuyển hết 132 gam chất béo trên thành chất rắn?
A. 0,3 gam.
B. 2,4 gam.
C. 4,5 gam.
D. 1,5 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
![]()
![]()
![]()
![]()
Số nguyên tử
![]()
CTPT là C57H100O6
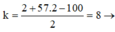
trong gốc hiđrocacbon có 5 liên kết pi
![]()

Gọi số mol của 440 g chất béo là b (mol)
\(\left(RCOO\right)_3C_3H_5+3NaOH->3RCOONa+C_3H_5\left(OH\right)_3\\ b=\dfrac{60}{40\cdot3}=0,5mol\\ M_{cb}=\dfrac{440}{0,5}=880\left(g\cdot mol^{-1}\right)\\ C_{cb}=\dfrac{28,5}{0,5}=57\\ CB:C_{57}H_{100}O_6,hay:C_nH_{2n-4-2k}O_6\left(k:số.lk.\pi.C=C.hoặc.C\equiv C\right)\\ 2.57-4-2k=100\\ k=5\\ n_{H_2}=kb=2,5mol\\ m_{H_2}=2,5.2=5g\)
Đồng đẳng hóa:
\(\left\{{}\begin{matrix}\left(HCOO\right)_3C_3H_5:a\\CH_2:b\\H_2:-c\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}m=176a+14b-2c=440\\n_{NaOH}=3a=\dfrac{60}{40}=1,5\\\dfrac{n_{cbeo}}{n_{CO_2}}=\dfrac{0,5}{28,5}=\dfrac{a}{6a+b}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=25,5\\c=2,5\end{matrix}\right.\)
Vậy \(m_{H_2}=2,5.2=5\left(g\right)\)

Chọn đáp án A
☆ giải đốt: m gam chất béo + 1,61 mol O2 → t o 1,14 mol CO2 + 1,06 mol H2O.
⇒ BTKL có m = 17,72 gam || bảo toàn nguyên tố O có nO trong chất béo = 0,12 mol.
mà chất béo có 6O ⇒ nchất béo = 0,12 ÷ 6 = 0,02 mol.
☆ 17,72 gam chất béo (0,02 mol) cần 0,06 mol NaOH → muối + 0,02 mol C3H5(OH)3.
||⇒ BTKL có mmuối = 17,72 + 0,06 × 40 – 0,02 × 92 = 18,28 gam

Chọn đáp án A
giải đốt:
m gam chất béo + 1,61 mol O2 ![]() 1,14 mol CO2 + 1,06 mol H2O.
1,14 mol CO2 + 1,06 mol H2O.
⇒ BTKL có m=17,72 gam
bảo toàn nguyên tố O có nO trong chất béo = 0,12 mol.
mà chất béo có 6O
⇒ nchất béo = 0,12 ÷ 6 = 0,02 mol.
17,72 gam chất béo (0,02 ml) cần 0,06 mol NaOH → muối + 0,02 mol C3H5(OH)3.
⇒ BTKL có
mmuối = 17,72 + 0,06 × 40 – 0,02 × 92 = 18,28 gam