chứa 0,394 mol HNO3, thu được dung dịch Y và V ml khí N2 (đktc). Dung dịch Y tác dụng vừa đủ với 1,94 lít dung dịch NaOH 0,25M để thu được dung dịch trong suốt. Giá trị của V gần nhất với giá trị nào sau đây?
A. 246,4
B. 268,7
C. 672,0
D. 896,0
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D.
Hỗn hợp X gồm Al (0,02 mol) và Zn (0,05 mol)
Dung dịch Y gồm Al3+ (0,02 mol), Zn2+ (0,05 mol), NH4+ (x mol), H+ (y mol), NO3- .Ta có:
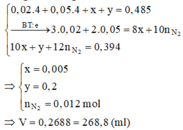

Chọn đáp án B
nAl = 0,02 mol; nZn = 0,05 mol; nNaOH = 0,485 mol.
NaOH + Y → dung dịch trong suốt {NaAlO2, Na2ZnO2, NaNO3}
Bảo toàn nguyên tố Natri: nNO3–/Y = nNaNO3 = 0,365 mol.
► Hòa tan "hoàn toàn" ⇒ HNO3 dư hoặc đủ, kim loại hết.
Đặt nNH4+ = x; nN2 = y. Bảo toàn electron:
8x + 10y = 0,02 × 3 + 0,05 × 2. Bảo toàn nguyên tố Nitơ:
∑nN/spk = 0,394 - 0,365 = x + 2y || Giải hệ có:
⇒ x = 0,005 mol; y = 0,012 mol ⇒ V = 268,8 ml ⇒ chọn B.

Chọn đáp án B
nAl = 0,02 mol; nZn = 0,05 mol; nNaOH = 0,485 mol.
NaOH + Y → dung dịch trong suốt {NaAlO2, Na2ZnO2, NaNO3}
Bảo toàn nguyên tố Natri: nNO3–/Y = nNaNO3 = 0,365 mol.
► Hòa tan "hoàn toàn" ⇒ HNO3 dư hoặc đủ, kim loại hết.
Đặt nNH4+ = x; nN2 = y. Bảo toàn electron:
8x + 10y = 0,02 × 3 + 0,05 × 2. Bảo toàn nguyên tố Nitơ:
∑nN/spk = 0,394 - 0,365 = x + 2y || Giải hệ có:
⇒ x = 0,005 mol; y = 0,012 mol ⇒ V = 268,8 ml ⇒ chọn B.

Giải thích:
![]()
![]()
=> Axit là HNO3
Dd Z chứa Al3+ và có thể có NH4+
NaOH + dd Z tạo ra dd trong suốt => NaOH hòa tan muối Al3+ thành AlO2-
nOH- = 4nAl3+ + nNH4+ => nNH4+ = 1,45 – 4.0,34 = 0,09 (mol)
Gọi k là số electron N+5 nhận để tạo ra khí Y
BT e: ne (Al nhường) = ne (N+5 nhận)
=> 0,34.3 = 0,03k + 0,09.8
=> k = 10
=> Y là N2
Áp dụng CT nhanh: nHNO3 = 12nN2 + 10nNH4+ = 12.0,03+ 10.0,09 = 1,26 (mol)
=> VHNO3 = 1,26.22,4 = 5,04 (lít)
Đáp án B

Đáp án B
nA = 9,18/27 = 0,34 (mol)
nY = 0,672/2,4 = 0,03 (mol)
nNaOH = 1,45 (mol)
=> Axit là HNO3
Dd Z chứa Al3+ và có thể có NH4+
NaOH + dd Z tạo ra dd trong suốt => NaOH hòa tan muối Al3+ thành AlO2-
nOH- = 4nAl3+ + nNH4+ => nNH4+ = 1,45 – 4.0,34 = 0,09 (mol)
Gọi k là số electron N+5 nhận để tạo ra khí Y
BT e: ne (Al nhường) = ne (N+5 nhận)
=> 0,34.3 = 0,03k + 0,09.8
=> k = 10
=> Y là N2
Áp dụng CT nhanh: nHNO3 = 12nN2 + 10nNH4+ = 12.0,03+ 10.0,09 = 1,26 (mol)
=> VHNO3 = 1,26.22,4 = 5,04 (lít)

Đáp án B
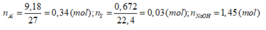
=> Axit là HNO3
Dd Z chứa Al3+ và có thể có NH4+
NaOH + dd Z tạo ra dd trong suốt
=> NaOH hòa tan muối Al3+ thành AlO2-
nOH- = 4nAl3+ + nNH4+
=> nNH4+ = 1,45 – 4.0,34 = 0,09 (mol)
Gọi k là số electron N+5 nhận để tạo ra khí Y
BT e: ne (Al nhường) = ne (N+5 nhận)
=> 0,34.3 = 0,03k + 0,09.8
=> k = 10
=> Y là N2
Đáp án : B
nAl = 0,02 ; nZn = 0,05 mol
Giả sử sau phản ứng có HNO3 dư và NH4NO3
=> nNaOH = 4nZn + 4nAl + nNH4NO3 + nHNO3 dư = 0,485
(dung dịch trong suốt => kết tủa tan)
nHNO3 = 2nZn + 3nAl + 2nNH4NO3 + nHNO3 dư + 2nN2 = 0,394
Bảo toàn e : 2nZn + 3nAl = 8nNH4NO3 + 10nN2
=> nN2 = 0,012 mol
=> V = 268,8ml