Cho 7,2 gam bột Mg tan hết trong dung dịch hỗn hợp HCl (dư) và KNO3, thu được dung dịch X chứa m gam muối và 2,688 lít khí Y (đktc) gồm N2 và H2 có khối lượng 0,76 gam. Giá trị của m là ?
A. 29,87
B. 24,03
C. 32,15
D. 34,68
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Đặt nN2 = x; nH2 = y || nY = x + y = 0,12 mol; mY = 28x + 2y = 0,76(g).
||⇒ giải hệ có: x = 0,02 mol; y = 0,1 mol. Bảo toàn electron: 2nMg = 10nN2 + 2nH2 + 8nNH4+.
⇒ nNH4+ = (2 × 0,3 - 10 × 0,02 - 2 × 0,1) ÷ 8 = 0,025 mol. Bảo toàn nguyên tố Nitơ:
nKNO3 = 0,025 + 0,02 × 2 = 0,065 mol. Do thu được H2 ⇒ X không chứa NO3–.
||⇒ X gồm các ion Mg2+, K+, NH4+ và Cl–. Bảo toàn điện tích: nCl– = 0,69 mol.
► m = 0,3 × 24 + 0,065 × 39 + 0,025 × 18 + 0,69 × 35,5 = 34,68(g) ⇒ chọn A

Đáp án A
Đặt nN2 = x; nH2 = y || nY = x + y = 0,12 mol; mY = 28x + 2y = 0,76(g).
|⇒ giải hệ có: x = 0,02 mol; y = 0,1 mol.
Bảo toàn electron: 2nMg = 10nN2 + 2nH2 + 8nNH4+.
⇒ nNH4+ = (2 × 0,3 - 10 × 0,02 - 2 × 0,1) ÷ 8 = 0,025 mol.
Bảo toàn nguyên tố Nitơ:
nKNO3 = 0,025 + 0,02 × 2 = 0,065 mol.
Do thu được H2 ⇒ X không chứa NO3–.
||⇒ X gồm các ion Mg2+, K+, NH4+ và Cl–.
Bảo toàn điện tích: nCl– = 0,69 mol.
► m = 0,3 × 24 + 0,065 × 39 + 0,025 × 18 + 0,69 × 35,5 = 34,68(g)

Đáp án A
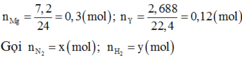
Ta có:
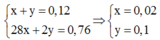
Ta thấy ne (khí nhận) = 0,02.10 + 0,1.2 = 0,4 < ne (nhường của Mg) = 0,3.2 = 0,6
Þ Tạo muối N H + 4


Đáp án A
nMg = 7,2: 24 = 0,3 (mol); nY = 2,688: 22,4 = 0,12 (mol)
Gọi nN2 = x (mol); nH2 = y (mol)
Ta có:
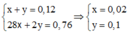
Ta thấy ne(khí nhận) = 0,02. 10 + 0,1.2 = 0,4 < ne (nhường của Mg) = 0,3. 2= 0,6
=> Tạo muối NH4+
nNH4+ = ( 0,3.2 – 0,02.10 – 0,1.2)/8 = 0,025 (mol)
m muối = mMgCl2 + m NH4Cl + mKCl
= 0,3. 95 + 0,025. 53,5 + ( 0,02.2+ 0,025). 74,5 = 34,68(g)

câu D mà.
giải:
N2:x, H2;y
-> x+y=0,12 (1)
28x+2y=0,76(2)
(1),(2): x=0,02; y=0.1
BTE: n e nhường(Mg)= 0,3.2=0.6
n e nhận= 0,02.10+0,1.2=0,4
=> Mg có tạo muối NH4+ với số mol NH4+=0,6-0,4/8=0,025
hh Y có H2 nên Mg còn duu sau phản ứng với NO3- => NO3- hết và toàn bộ muối chuyển thành muối Cl-
muối: MgCl2, NH4Cl, KCl
số K+ được tính theo NO3-
BTNT N: 0,02.2+0,025.1=0.065
m= 0,3.95+0,025.53,5+0,065.74,5
= 34,68
nY=0,12 mol => MY= 19/3 (g/mol) áp dung quy tắc đường chéo => nH2= 0,1mol và nN2=0,02mol Bảo toàn e ta có: 2H+ + 2e => H2 12H+ + 2NO3- + 10e => N2 + 6H2O
nHCl PƯ= nH+ = 0,24+0,2=0,44 mol nKNO3=0,04 mol
m Muối= mMg+mHCl+mKNO3-mH2-mN2-mH2O=24,38(g)

Đáp án C
Từ nHỗn hợp 2 khí và khối lượng 2 khí
⇒ nN2 = 0,01 và nH2 = 0,1 mol.
Bảo toàn e ta có nNH4+ = ![]() = 0,025 mol.
= 0,025 mol.
⇒ nHCl = 12nN2 + 2nH2 + 10nNH4+ = 0,69 mol.
+ Bảo toàn điện tích hoặc bảo toàn nitơ
⇒ nK+ = 0,065 mol.
⇒ mMuối = 0,3×24 + 0,065×39 + 0,025×18 + 0,69×35,5
= 34,68 gam.

Đáp án C
Từ nHỗn hợp 2 khí và khối lượng 2 khí ⇒ nN2 = 0,01 và nH2 = 0,1 mol.
Bảo toàn e ta có nNH4+
![]()
⇒ nHCl = 12nN2 + 2nH2 + 10nNH4+ = 0,69 mol.
Sơ đồ bài toán:
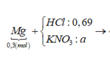
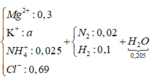
+ Bảo toàn điện tích hoặc bảo toàn nitơ ⇒ nK+ = 0,065 mol.
⇒ mMuối = 0,3×24 + 0,065×39 + 0,025×18 + 0,69×35,5 = 34,68 gam.
Đáp án : D