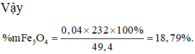Dung dịch X gồm 0,015 mol Cu(NO3)2 và 0,16 mol KHSO4. Khối lượng Fe tối đa phản ứng được với dung dịch X là (biết NO là sản phẩm khử duy nhất của NO3-)
A. 3,36 gam
B. 4,48 gam
C. 2,99 gam
D. 8,96 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Số mol các chất là:
![]()
![]()
Lượng Fe phản ứng tối đa => Thu được khí H2 và dung dịch sau phản ứng chỉ có ![]()
![]()
![]()
![]()
![]()
![]()
Các quá trình tham gia của H+:
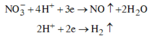
![]()
![]()
![]()
![]()
Đáp án D

Chọn đáp án B
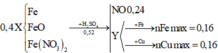
Y có thể gồm các ion thuộc 1 trong 3 trường hợp:
TH1: Fe2+ (có thể), Fe3+, H+, S O 4 2 -
TH2: Fe2+ (có thể), N O 3 - , S O 4 2 -
TH3: Fe3+, H+, N O 3 - , S O 4 2 -
Lượng Cu và Fe hoà tan tối đa là như nhau Þ Chỉ có thể là TH2 hoặc TH3 vì TH1 có H+ mà không
có N O 3 - Þ Tạo thêm H2, làm cho lượng Fe tối đa hoà tan được nhiều hơn Cu
nCu max = nFe max = 0,16 Þ Số mol Fe3+ trong Y tối đa = 0,16x2 = 0,32
Với TH3 thì nFe3+ = 0,4 Þ Chỉ có TH2 thỏa mãn Y
Trong đó Y chứa: Fe3+ (0,32 mol), Fe2+ (0,08 mol), N O 3 - , S O 4 2 - (0,52 mol)
BTĐT Þ nNO = 0,32x3 + 0,08x2 - 0,52x2 = 0,08
Bán phản ứng Þ nFeO = (0,52x2 - 0,24x4)/2 = 0,04
BTNT.N Þ nFe(NO3)2 = (0,24 + 0,08)/2 = 0,16 Þ nFe = 0,4 - 0,16 - 0,04 = 0,2
Vậy %Fe(NO3)2 = ![]()

Chọn đáp án D
Y có thể hoà tan được Cu và Fe sinh ra NO ⇒ Còn dư H+ và N O 3 - trong Y
⇒ Dung dịch Y gồm: Fe3+, H+, N O 3 - và S O 2 -

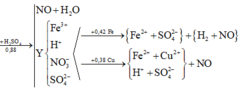
Y hoà tan tối đa 0,42 mol Fe nhưng chỉ hoà tan tối đa 0,38 mol Cu, sự chênh lệch này là do Cu không tác dụng với H+ tạo H2, đặt Z là dung dịch sau khi Y phản ứng với Cu