Cho cân bằng hóa học sau: 2NH3 (k) ⇆ N2 (k) + 3H2 (k). Khi tăng nhiệt độ của hệ thì tỉ khối của hỗn hợp so với H2 giảm. Nhận xét nào sau đây là đúng?
A. Khi tăng áp suất của hệ, cân bằng chuyển dịch theo chiều thuận
B. Khi tăng nhiệt độ của hệ, cân bằng chuyển dịch theo chiều thuận
C. Phản ứng thuận là phản ứng tỏa nhiệt
D. Khi tăng nồng độ của NH3, cân bằng chuyển dịch theo chiều nghịch


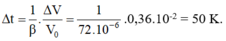
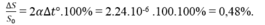
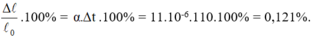
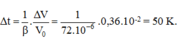
Chọn B
Theo giả thiết : Khi tăng nhiệt độ của hệ thì tỉ khối của hỗn hợp so với H2 giảm. Suy ra khối lượng trung bình của hỗn hợp giảm. Mặt khác, khối lượng hỗn hợp không thay đổi. Suy ra số mol khí tăng lên, tức là cân bằng đã chuyển dịch theo chiều thuận.
Vậy nhận xét đúng là : "Khi tăng nhiệt độ của hệ, cân bằng chuyển dịch theo chiều thuận".