Điện phân 100 ml dung dịch CuSO4 0,2 M và AgNO3 0,1 M với cường dòng điện I = 3,86 A. trong thời gian t giây thì thu được một khối lượng kim loại bám bên catot là 1,72g. Giá trị của t là
A. 750s
B. 1000s
C. 500s
D. 250s
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Dạng thời gian t, 2t kết hợp với khối lượng dung dịch giảm. ► quy cái này giải cho dễ này:
dung dịch giảm MO hay M2O hay M2O3 quy hết về dạng MnO nhé (n = 1 hoặc 2 hoặc 2/3 tùy).
• xét thời gian t (giây): dung dịch giảm x mol MnO ⇄ 6,96 gam → ne trao đổi = 2x mol.
thời gian 2t (giây) → ne trao đổi = 4x mol; catot ra 0,01 mol H2 → ứng với dung dịch ra 0,01 mol H2O.
→ 11,78 gam dung dịch giảm gồm 0,01 mol H2O và còn (2x – 0,01) mol MnO nữa.
→ Phương trình: 11,78 = 0,01 × 18 + 2 × 6,96 – 0,01 × MMnO → MnO = 232.
→ nM = 216 ứng với cặp n = 2 và M = 108 là kim loại Ag.
Thay ngược lại → x = 6,96 ÷ 232 = 0,03 mol → a = 6,48 gam

Chọn đáp án C.
Trong t (s)
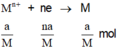
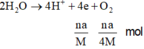
⇒ mdung dịch giảm = a + 32 n a 4 M = 6 , 96
a + 8 n a M = 6 , 96 (1)
Trong 2t (s) ⇒ ne trao đổi = 2 n a M
Tại catot:
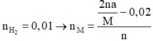
Tại anot:
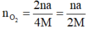
⇒ mdung dịch giảm = 11 , 78
![]()
Từ (1) và (2)
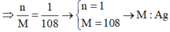
![]()

Đáp án C
Dạng thời gian t, 2t kết hợp với khối lượng dung dịch giảm. ► quy cái này giải cho dễ này:
dung dịch giảm MO hay M2O hay M2O3 quy hết về dạng MnO nhé (n = 1 hoặc 2 hoặc 2/3 tùy).
• xét thời gian t (giây): dung dịch giảm x mol MnO ⇄ 6,96 gam → ne trao đổi = 2x mol.
thời gian 2t (giây) ||→ ne trao đổi = 4x mol; catot ra 0,01 mol H2 → ứng với dung dịch ra 0,01 mol H2O.
||→ 11,78 gam dung dịch giảm gồm 0,01 mol H2O và còn (2x – 0,01) mol MnO nữa.
||→ Phương trình: 11,78 = 0,01 × 18 + 2 × 6,96 – 0,01 × MMnO ||→ MnO = 232.
||→ nM = 216 ứng với cặp n = 2 và M = 108 là kim loại Ag.
Thay ngược lại → x = 6,96 ÷ 232 = 0,03 mol → a = 6,48 gam
Đáp án : A
Ag+ bị điện phân trước
Giả sử kim loại có Ag và Cu => nAg = 0,01 mol => nCu = 0,01 mol
=> ne trao đổi = 2nCu + nAg =It/F
=> t = 750s