Cho 38,4 gam hỗn hợp Fe, FeO, Fe3O4 tác dụng với 2,4 mol HNO3 (dư) trong dung dịch, thu được V lít khí NO (sản phẩm khử duy nhất, đktc) và dung dịch X. Dung dịch X phản ứng với 1400 ml dung dịch NaOH 1M thu được 42,8 gam kết tủa. Giá trị của V là
A. 8,96
B. 6,72
C. 11,2
D. 3,36



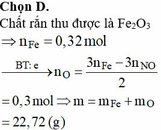

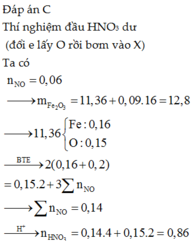

Chọn đáp án A
HNO3 dùng dư nên dung dịch X thu được gồm Fe(NO3)3 và HNO3 còn dư.
NaOH phản ứng với X: NaOH + HNO3 → NaNO3 + H2O.
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ + 3NaNO3.
Có 42,8 gam Fe(OH)3↓ ⇔ 0,4 mol mà ∑nNaOH = 1,4 mol
⇒ nHNO3 còn dư trong X = 1,4 – 0,4 × 3 = 0,2 mol. Rút gọn lại:
38,4 gam (Fe; O) + 2,2 mol HNO3 → Fe(NO3)3 + NO + H2O.
Gọi nFe = x mol; nO = y mol ||⇒ 56x + 16y = 38,4 gam.
Bảo toàn electron có: 3nFe = 2nO + 2nNO ⇒ nNO = (3x – 2y) ÷ 3 mol.
Bảo toàn nguyên tố N có: nHNO3 = nN trong Fe(NO3)3 + nNO.
⇒ thay số có: 3x + (3x – 2y) ÷ 3 = 2,2 mol ⇒ giải x = 0,6 mol và y = 0,3 mol.
Thay lại có nNO = (3x – 2y) ÷ 3 = 0,4 mol ⇒ V = 0,4 × 22,4 = 8,96 lít. Chọn đáp án A