Cho 5,2g hỗn hợp gồm Al, Mg và Zn tác dụng vừa đủ với dung dịch H 2 S O 4 10% thu được dung dịch Y và 3,36 lít khí H 2 (đktc). Khối lượng của dung dịch Y là
A. 152g.
B. 146,7g.
C. 175,2g.
D. 151,9g.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D
nH2SO4 = nH2 = 0,15 ⇒ mdd H2SO4 = 0,15.98/10% = 147g
Bảo toàn khối lượng ⇒ mdd Y = 5,2 + 147 – 0,15.2 = 151,9g

Đáp án D
nH2SO4 = nH2 = 0,15 => mdd H2SO4 = 0,15.98/10% = 147g
Bảo toàn khối lượng => mdd Y = 5,2 + 147 – 0,15.2 = 151,9g

Số mol H2 là: ![]()
Gọi M là kim loại chung cho Al, Mg, Zn với hóa trị n
Sơ đồ phản ứng: 
![]()
![]()


![]()
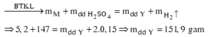
Đáp án D

Chọn C
BTNT H: nH2SO4 = nH2 = 0,15 mol => m (dd H2SO4 10%) = 0,15.98.(100/10) = 147 gam
KL + dd H2SO4 → muối + H2
BTKL: m muối = mKL + m (dd H2SO4 10%)– mH2 = 5,2 + 147 – 0,15.2 = 151,9 gam

Đáp án C
BTNT H: nH2SO4 = nH2 = 0,15 mol
=> m (dd H2SO4 10%) = 0,15.98.(100/10) = 147 gam
KL + dd H2SO4 → muối + H2
BTKL:
m muối = mKL + m (dd H2SO4 10%)– mH2 = 5,2 + 147 – 0,15.2 = 151,9 gam

Giải thích: Đáp án C
BTNT H: nH2SO4 = nH2 = 0,15 mol => m (dd H2SO4 10%) = 0,15.98.(100/10) = 147 gam
KL + dd H2SO4 → muối + H2
BTKL: m muối = mKL + m (dd H2SO4 10%)– mH2 = 5,2 + 147 – 0,15.2 = 151,9 gam

Đáp án C
BTNT H: nH2SO4 = nH2 = 0,15 mol => m (dd H2SO4 10%) = 0,15.98.(100/10) = 147 gam
KL + dd H2SO4 → muối + H2
BTKL: m muối = mKL + m (dd H2SO4 10%)– mH2 = 5,2 + 147 – 0,15.2 = 151,9 gam
Đáp án D
nH2SO4 = nH2 = 0,15 => mdd H2SO4 = 0,15.98/10% = 147g
Bảo toàn khối lượng => mdd Y = 5,2 + 147 – 0,15.2 = 151,9g