Hòa tan hoàn toàn m gam Al bằng dung dịch HNO3 loãng, thu được 5,376 lít (đktc) hỗn hợp khí X gồm N2, N2O và dung dịch chứa 8m gam muối. Tỉ khối của X so với H2 bằng 18. Giá trị của m là
A. 17,28
B. 19,44
C. 18,90
D. 21,60
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Đặt n N 2 = x , n N 2 O = y ⇒ n X = x y = 0 , 24 m o l
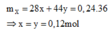
Bảo toàn e:
3 n A l = 10 n N 2 + 8 n N 2 O + 8 n N H 4 N O 3
⇒ n N H 4 N O 3 = ( m / 72 - 0 , 72 ) m o l
⇒ muối gồm A l ( N O 3 ) 3 ; N H 4 N O 3
![]()
⇒ m = 21 , 6 ( g )

Đáp án B
nAl = m/27 => mAl(NO3)3 = 213.m/27 = 71m/9 < 8m
=> mNH4NO3 = 8m – 71m/9 = m/9 => nNH4NO3 = m/720

Bảo toàn ne => 3nAl = 10nN2 + 8nN2O + 8nNH4NO3
=> 3m/27 = 10.0,12 + 8.0,12 + 8m/720 => m = 21,6

Đáp án B
nAl = m/27 => mAl(NO3)3 = 213.m/27 = 71m/9 < 8m
=> mNH4NO3 = 8m – 71m/9 = m/9=> nNH4NO3 = m/720
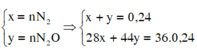
![]()
Bảo toàn ne =>3nAl = 10nN2 + 8nN2O + 8nNH4NO3
=>3m/27 = 10.0,12 + 8.0,12 + 8m/720=> m = 21,6=> Chọn B.
Dạng bài KL có tính khử mạnh như Al, Mg… tác dụng với HNO3 (hoặc H2SO4) cần chú ý sản phẩm có thể có muối NH4NO3.
- Ta có hệ:
nN2 + nN2O = 0.24 mol
28nN2 + 44nN2O = 0.24*18*2 g
=> nN2 = 0.12 mol; nN2O = 0.12 mol
- Bảo toàn electron cho phản ứng:
3nAl = 10nN2 + 8nN2O + 8nNH4NO3
=> 3*m/27 = 10*0.12 + 8*0.12 + 8*nNH3NO3
=> nNH3NO3 = m/72 – 0.27 (mol)
- Khối lượng muối tạo thành: mmuối = mAl(NO3)3 + mNH3NO3
=> 8m = 213*(m/27) + 80*( m/72 – 0.27)
=> m = 21.6 g
=> Đáp án D