Tiến hành điện phân (điện cực trơ, mằng ngăn xốp) một dung dịch chứa m gam hỗn hợp CuSO4 và NaCl cho tới khi nước bắt đầu bị điện phân ở cả hai điện cực thì dừng lại. Ở anot thu được 0,448 lít khí (đktc). Dung dịch sau điện phân có thể hòa tan tối đa 0,68g Al2O3. Giá trị m có thể là giá trị nào sau đây?
A. 11,94 gam
B. 4,47 gam
C. 8,94 gam
D. 9,28 gam


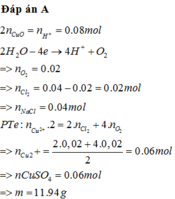

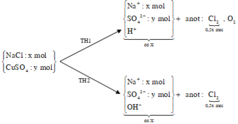

Nhận thấy dung dịch sau điện phân có thể hòa tan Al2O3 → dung dịch sau phản ứng hoặc chứa ion H+,
hoặc chứa ion OH-
Nếu dung dịch sau phản ứng chứa ion H+ → bên anot sinh ra khí O2 và Cl2-
→nH2+ = 6n Al2O3 = 0,04 mol → n O2 = n H+ : 4 = 0,01 mol → n Cl2 = 0,02 – 0,01 = 0,01 mol → n NaCl = 0,02 mol
Bảo toàn electron → 2nCu = 4nO2 + 2nCl2 → nCu = nCuSO4 = 0,03 mol
m= mCuSO4 + mNaCl = 5,97 gam
TH2: Dung dịch sau phản ứng chứa ion OH- → bên anot chỉ sinh ra khí Cl2.
nOH- = 2nAl2O3 = 1/75 mol → nH2 = 1/50 mol
→ nCl2 = 0,02 mol → nNaCl = 0,04 mol
Bảo toàn electron → 2.nCuSO4 = 2nCl2 - 2nH2 → nCuSO4= 1/75mol
m = mCuSO4 + mNaCl = 1/75 .160 + 0,04.58,5= 4,473.=>B