Cho từ từ từng giọt đến hết 100 ml dung dịch HCl aM vào 100 ml dung dịch Na2CO3 1M, thấy thoát ra 1,344 lít khí CO2 (đktc). Giá trị của a là
A. 1,6
B. 0,8
C. 0,6
D. 1,2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
nH+ = 0,2 < 0,15 x 2 + 0,1 → CO2 chưa đạt số mol tối đa
Nhỏ từ từ H+ vào dung dịch hỗn hợp 2 muối thì phản ứng xảy ra đồng thời theo đúng tỉ lệ số mol ban đầu. Ban đầu có nCO32- /nHCO3– =3/2
Đặt số mol phản ứng của CO32- là 3a → Số mol HCO3– phản ứng là 2a
nH+ phản ứng = 2 x 3a + 2a = 0,2 → a = 0,025 → nCO2 = 3a + 2a = 0,125
Vậy V = 0,125 x 22,4 = 2,8.

Ta có nCO32- = nNa2CO3 = 1,5.0,1 = 0,15 mol; nHCO3-bđ = nKHCO3 = 1.0,1 = 0,1 mol
nH+ = nHCl = 1.0,2 = 0,2 mol
Khi cho từ từ HCl vào dung dịch X thì phản ứng xảy ra theo trình tự:
H+ + CO32- → HCO3-(1)
0,15 mol ← 0,15 mol → 0,15 mol
⇒ nH+còn dư = 0,2 – 0,15 = 0,05 mol; nHCO3- mới = 0,15 + 0,1 = 0,25 mol
H+còn dư + HCO3- → CO2↑ + H2O (2)
(0,05) (0,25) → 0,05
⇒ V = 0,05.22,4 = 1,12 lít ⇒ Chọn B.

Đáp án B
Số mol CO32- = 0,15 (mol) ; số mol HCO3- = 0,1(mol) ; số mol H+=0,2(mol)
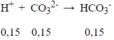
Tổng số mol HCO3- = 0,25 ;
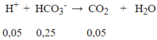
⇒ VCO2 = 0,05.22,4=1,12 (lít)
Đáp án A