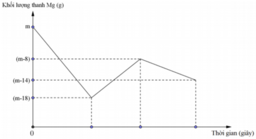
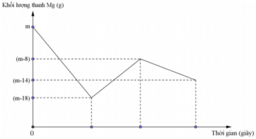
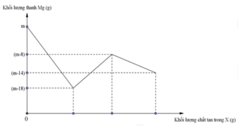
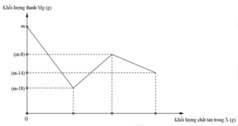
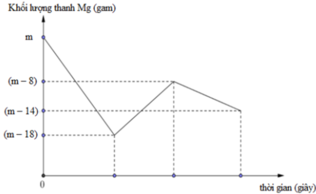
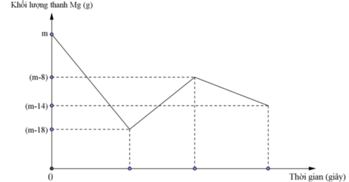
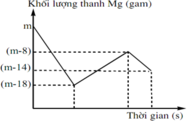
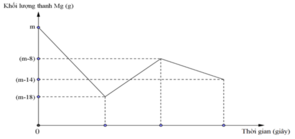
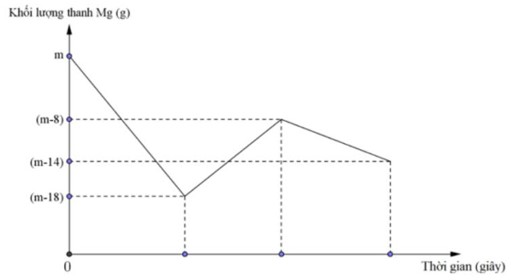
Đồ thị biểu diễn sự phụ thuộc của khối lượng Mg vào dung dịch hỗn hợp X chứa a mol muối Cu(NO3)2 và b mol HCl khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X được biểu diễn như hình vẽ dưới đây: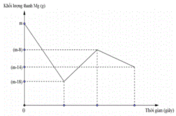
Sau khi phản ứng xảy ra hoàn toàn lấy thanh Mg ra, thu được khí NO là sản phẩm khử duy nhất của N+5. Tỉ lệ a : b là
A. 1 : 8.
B. 8 : 1.
C. 1 : 10
D. 10 : 1