Cho V1 ml dung dịch NaOH 0,4M vào V2 ml dung dịch H2SO4 0,6M. Sau khi kết thúc phản ứng thu được dung dịch chỉ chứa một chất tan duy nhất. Tỉ lệ V1 : V2 là
A. 1 : 3
B. 3 : 2
C. 3 : 1
D. 2 : 3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Chất tan duy nhất là Na2SO4 do đó: 0,4V1=0,6V2.2 suy ra V1=3V2

Chọn đáp án B
Xét thí nghiệm 1: 3Ba(OH)2 + Al2(SO4)3 → 3BaSO4 + 2Al(OH)3.
Giả sử
![]()
Phản ứng vừa đủ ⇒ n B a ( O H ) 2 = 3 V 1
![]()
![]()
⇒ 0 , 9 m = 769 , 5 V 1 g a m
s TH1: Ba(OH)2 thiếu. n B a ( O H ) 2 = V 2 mol
![]()
![]()
![]()
s TH2: Ba(OH)2 dư, hòa tan 1 phần Al(OH)3. Khi đó:
3Ba(OH)2 + Al2(SO4)3 → 3BaSO4 + 2Al(OH)3 (1)
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O (2)
Từ (1)
![]()
![]()
![]()
![]()
![]()

Định hướng tư duy giải
Ta có:
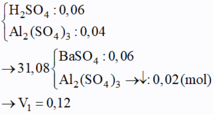
Thêm tiếp Ba(OH)2 kết tủa bị tan 1 phần
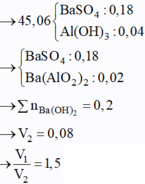

Chọn A.
Vì V3 là lớn nhất nên dung dịch (2), (3) là hai axit Þ (1) là dung dịch chứa muối nitrat.
Phương trình ion: 4H+ + NO3- + 3e → NO + 2H2O
Đáp án C
Chất tan duy nhất là Na2SO4 do đó: 0,4V1=0,6V2.2 suy ra V1=3V2.