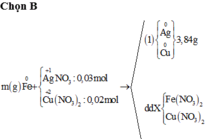
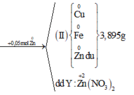
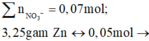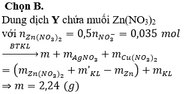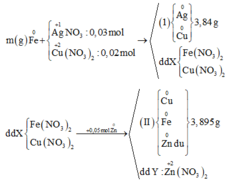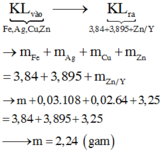Cho 4,23 gam hỗn hợp Mg và Al vào dung dịch chứa AgNO3 0,84M và Cu(NO3)2 0,96M, sau khi các phản ứng xảy ra hoàn toàn, thu được 23,12 gam hỗn hợp kim loại và dung dịch X chứa m gam muối. Cho X phản ứng hoàn toàn với dung dịch NaOH loãng (dư), thu được 10,39 gam kết tủa. Bỏ qua sự thủy phân của muối trong dung dịch. Giá trị của m gần nhất với giá trị nào sau đây?
A. 32.
B. 33.
C. 34.
D. 35.