Cho 4,48 lít khí CO2 (ở đktc) hấp thụ hết vào 100 ml dung dịch chứa hỗn hợp NaOH 1M và Ba(OH)2 1M, thu được m gam kết tủa. Giá trị của m là
A. 7,88.
B. 19,70.
C. 39,4.
D. 3,94.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNaOH = nBa(OH)2 = 0,1
→ n O H - = 0,3
nCO2 = 0,2—> nCO32- = nHCO3- = 0,1
—> nBaCO3 = 0,1
—> mBaCO3 = 19,7 gam
Đáp án D

Đáp án B
Ta có nCO2 = 0,2 mol và ∑nOH– = 0,3 mol.
⇒ nCO32– = ∑nOH– – nCO2 = 0,3 – 0,2 = 0,1 mol.
+ Lại có nBa2+ = 0,1 mol ⇒ nBaCO3↓ = 0,1 mol.
⇒ mKết tủa = mBaCO3 = 0,1×197 = 19,7 gam

Chọn D
Ta có: T = n O H - n C O 2 = 0 , 03 0 , 02 = 1 , 5 . Do đó có các quá trình sau xảy ra:
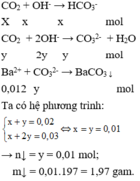

Đáp án A
Ta có nCO2 = 0,02 mol; nNaOH = 0,006 mol; nBa(OH)2 = 0,012 mol
nBa2+ = nBa(OH)2 = 0,012 mol và ∑nOH- = nNaOH + 2nBa(OH)2 = 0,006 + 2.0,012 = 0,03 mol
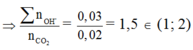
nên tạo ra 2 loại muối
nCO32- = nOH- - nCO2 = 0,03 – 0,02 = 0,01 mà nBa2+ = 0,012 mBaCO3↓ = 0,01.197 = 1,97g

Đáp án D
nOH-=0,006 + 2.0,012 = 0,03(mol)
nCO2 = 0,02(mol)
Có: 1 < n O H - n C O 2 < 2 nên tạo ra 2 ion số mol bằng nhau = 0,01mol
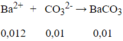
Khối lượng kết tủa = 0,01.197=1,97(g)

Đáp án C
nCO2 = 0,448: 22,4 = 0,02 mol
nOH = nNaOH + 2nBa(OH)2 = 0,1.0,06 + 2.0,1.0,12 = 0,03 mol
nBa2+ = 0,1.0,12 = 0,012 mol
Ta thấy nCO2 < nOH < 2nCO2
=> phản ứng tạo 2 muối
=> nCO3 = nOH – nCO2 = 0,03 – 0,02 = 0,01 mol < nBa2+
=> nBaCO3 = nCO3 = 0,01 mol
=> mBaCO3 = 0,01.197 = 1,97g
Đáp án B
Ta có nCO2 = 0,2 mol và ∑nOH– = 0,3 mol.
⇒ nCO32– = ∑nOH– – nCO2 = 0,3 – 0,2 = 0,1 mol.
+ Lại có nBa2+ = 0,1 mol ⇒ nBaCO3↓ = 0,1 mol.
⇒ mKết tủa = mBaCO3 = 0,1×197 = 19,7 gam