Hỗn hợp X có tỉ khối so với H2 là 27,8 gồm butan, metylxiclopropan, but-2-en, etylaxetilen và đivinyl. Khi đốt cháy hoàn toàn 0,15 mol X, tổng khối lượng của CO2 và H2O thu được là:
A. 34,50 g.
B. 36,66 g.
C. 37,20 g
D. 39,90 g.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MX = 21,2.2 = 42,4 ⇒ mX = 0,1.42,4 = 4,24g
X gồm các chất chứa 3 C trong phân tử
⇒ nCO2 = 3nX = 3. 0,1 =0,3
mH = mX – mC = 4,24 – 0,3.12 = 0,64 ⇒ nH2O = 0,32
⇒ mCO2 + mH2O = 0,3.44 + 0,32.18 = 18,96g
Đáp án B.

- Đặt CTTQ của X là ![]()
- Có ![]()
- Suy ra: ![]()
- Bảo toàn nguyên tố C => Số mol CO 2 = 0,15 (mol); bảo toàn nguyên tố H => Số mol H 2 O = 0,16 (mol)
- Vậy tổng khối lượng của CO 2 và H 2 O thu được là: 0,15.44 + 0,16.18 = 9,48 gam.
- Chọn đáp án B.

Ta có M ¯ của C3H8, C3H6 và C3H4 là 21,2.2 = 42,4
Gọi công thức trung bình của X là
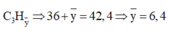
Ta có C3H6,4 → 3CO2 + 3,2H2O
0,1 mol → 0,3 → 0,32
=>mCO2 + mH2O = 44.0,3 + 18.0,32 = 18,96g
=>Chọn B.

Đáp án A
Hướng dẫn
nCO2 = 3nX = 3.0,1 = 0,3 mol; mX = 0,1.21.2 = 4,2 gam
=> nH2O = (4,2 – 0,3.12)/2 = 0,3 mol
m = mCO2 + mH2O = 0,3.44 + 0,3.18 = 18,6 gam
Các chất tham gia cấu tạo X trong phân tử đều có 4C.
Ta quy hỗn hợp đầu thành hỗn hợp C (0,6 mol) và H (a mol)
Ngoài ra ta có thể giải bài toán này bằng phương pháp trung bình.
Đáp án B