Hòa tan hoàn toàn 23,4 gam G gồm Al, Ni, Cu bằng dung dịch H2SO4 đặc nóng, thu được 15,12 lít khí SO2 (đktc). Nếu cho 23,4 gam G tác dụng hoàn toàn với dung dịch AgNO3 thì thấy khối lượng chất rắn tăng m% so với khối lượng G. Giá trị của m là:
A. 623,08
B. 311,54
C. 523,08
D. 411,54

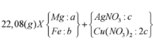
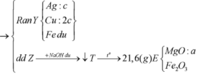
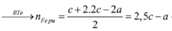
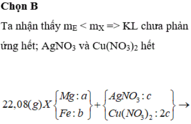
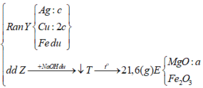
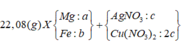
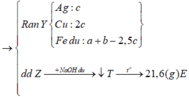
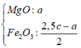
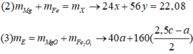
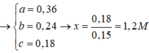
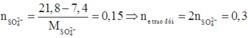
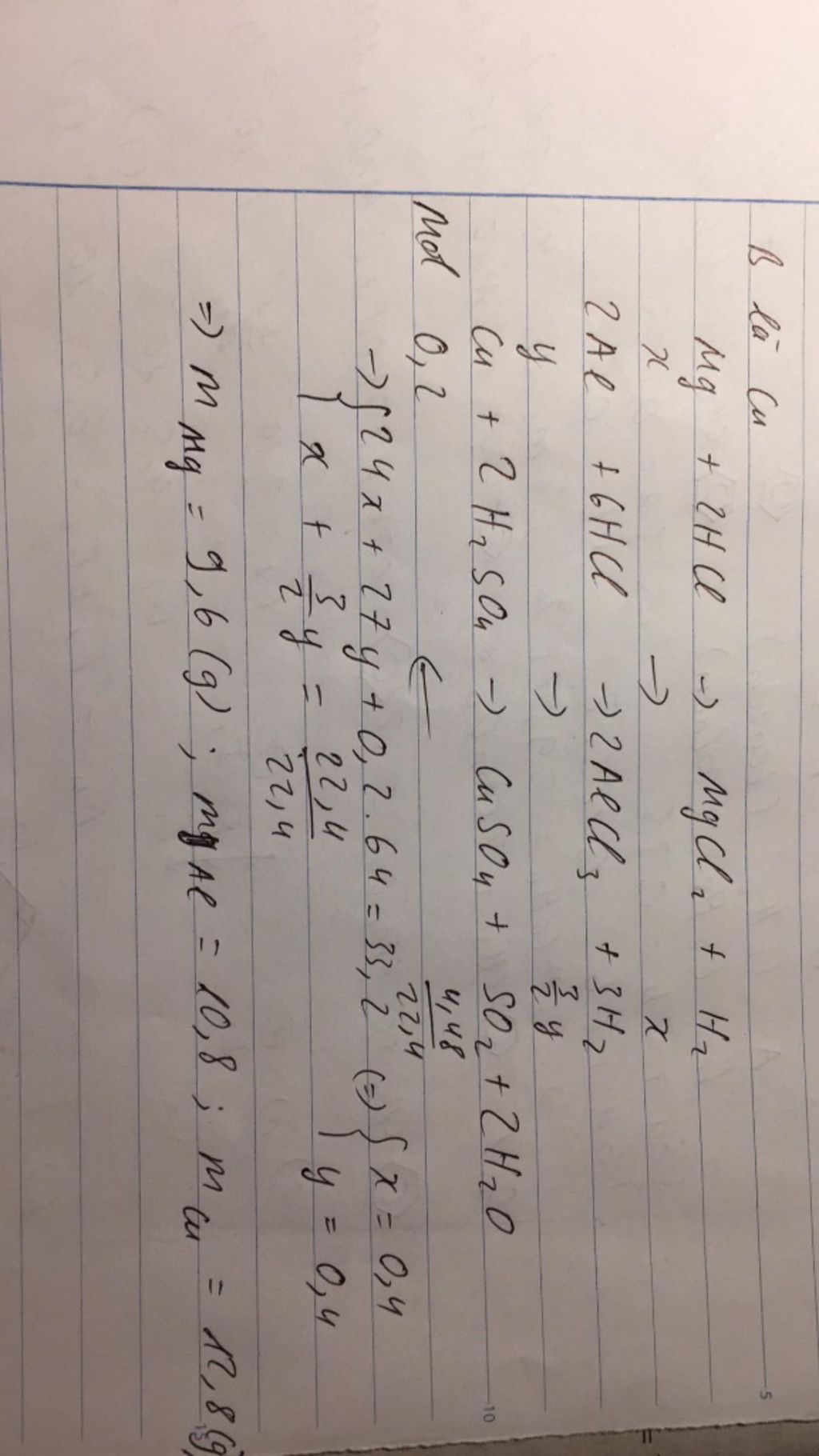

Đáp án C
Tương tự các bài trước, theo định luật bào toàn mol electron, ta có:
Mà đề bài hỏi khối lượng chất rắn tăng bao nhiêu phần trăm so với khối lượng G
Nên m = 623,08 – 100 = 523,08