Cho một mẫu hợp kim Na-K-Ba tác dụng với nước (dư), thu được dung dịch X và 0,784 lít H2 (ở đktc). Thể tích dung dịch axit HCl 0,5M cần dùng để trung hoà dung dịch X là
A. 150ml
B. 140ml
C. 200ml
D. 70ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
M + nH2O → M(OH)n + n 2 H2.
Ta có: n H 2 = 0,035 mol → n O H - = 0,07 mol → n H + = 0,07 → V = 0,07 : 0,5 = 0,14 lít

Đáp án C
M + nH2O → M(OH)n + n/2 H2.
Ta có: n(H2) = 0,035 mol → n(OH-) = 0,07 mol
→ n(H+) = 0,07
→ V = 0,07 : 0,5 = 0,14 lít

Đáp án B
Na + H2O → NaOH + H2 (1)
Ba + 2H2O → Ba(OH)2 + H2 (2)
Theo (1) và (2) n OH - ( dd X ) = 2 n H 2 = 0 , 3 mol
Phương trình ion rút gọn của dung dịch axit với dung dịch bazơ là
H+ + OH- → H2O
⇒ n H + = n OH - = 0 , 3 mol → n H 2 SO 4 = 0 , 15 mol
⇒ V H 2 SO 4 = 0 , 15 2 = 0 , 075 lit
=> Đáp án B

Chọn A.
Hợp kim K - Ca tan trong nước tạo dung dịch kiềm, đặt hợp kim K - Ca là M:
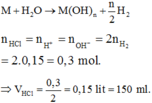
Chọn B.
M + nH2O → M(OH)n + n/2 H2.
Ta có: n(H2) = 0,035 mol → n(OH-) = 0,07 mol → n(H+) = 0,07 → V = 0,07 : 0,5 = 0,14 lít