Điện phân 225ml dung dịch AgNO3 1M với điện cực trơ trong thời gian t giờ, cường độ dòng điện không đổi 4,02A (hiệu suất quá trình điện phân đạt 100%) thu được chất rắn X, dung dịch Y và khí Z. Cho 18,9 gam bột Fe vào dung dịch Y, sau khi phản ứng kết thúc thu được 21,75 gam chất rắn T và khí NO (sản phẩm khử duy nhất của N+5. Phát biểu nào sau đây là sai ?
A. Chất rắn T thu được gồm 2 kim loại
B. Do Y có chứa HNO3 nên dung dịch sau điện phân có pH < 7
C. Trước khi cho sắt vào, nước ở catot chưa bị điện phân
D. Quá trình điện phân được tiến hành trong 5600 giây

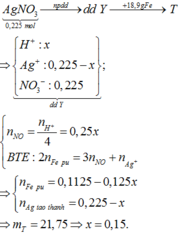



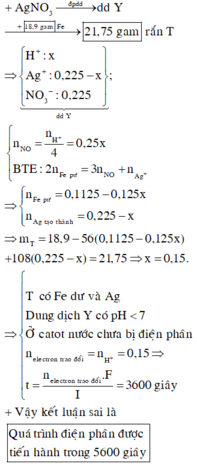
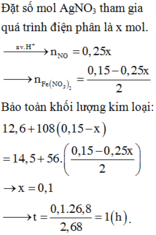
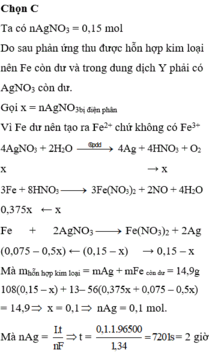
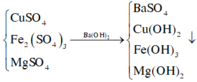
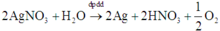
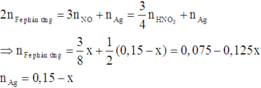
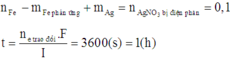
Chọn đáp án D