Điện phân (với điện cực trơ) dung dịch muối sunfat của một kim loại hóa trị II với I = 3A. Sau 1930 giây điện phân thấy khối lượng catot tăng 1,92g. Kim loại đó là
A. Zn.
B. Ba.
C. Ca.
D. Cu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

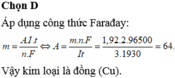

Đáp án A
Quá trình điện phân: M2+ + 2e → M
Có: ne = I.t/F = 3.1930/96500 = 0,06 mol
=> nM = ½ ne = 0,03 mol
=> MM = 1,92: 0,03 = 64 (g/mol) => Cu

Theo định luật Faraday ta có khối lượng chất thoát ra ở điện cực là :
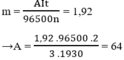
Trong đó A là nguyên tử khối
A = 64 ⇒ A là Cu

\(a.Catot:M^{2+}+2e\rightarrow M\\ Anot:2H_2O\rightarrow4H^++O_2+4e\\ PTHH:2MSO_4+2H_2O-^{đp}\rightarrow2M+O_2+2H_2SO_4\\ b.m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,92\\ \Rightarrow A=64\left(Cu\right)\)

\(m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,95=>A=65\left(Zn\right)\)

Có \(m=\dfrac{AIt}{nF}=\dfrac{A.6.9650}{3.96500}=11,2=>A=56\left(g/mol\right)\)
=> Muối đã điện phân là Fe2(SO4)3