Đốt cháy hoàn toàn một lượng E thu được 0,86 mol khí CO2 và 0,64 mol hơi nước. Mặt khác, thủy phân 93,2 gam E bằng 400 gam dung dịch NaOH 12% rồi cô cạn dung dịch thu được phần hơi Z có chứa chất hữu cơ T. Dẫn toàn bộ Z vào bình đựng Na, sau phản ứng khối lượng bình tăng 377,7 gam đồng thời thoát ra 12,32 lít khí H2 (đktc). Biết tỉ khối của T so với H2 là 16. Phần trăm khối lượng của Y trong hỗn hợp E có giá trị gần nhất với giá trị nào sau đây
A. 46,35%
B. 48,0%
C. 41,3%
D. 46,5%


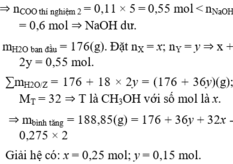














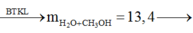
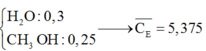
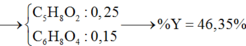
Đáp án A
TN1: Lượng este mang đốt cháy gồm:
X: CnH2n-2O2 (a mol)
Y: CmH2m-4O4 (b mol)
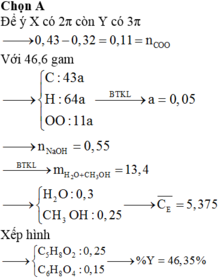
nCO2=an+bm=0,86 (1)
nH2O=(n-1)a+(m-2)b=0,64
=>a+2b=0,22 (2)
TN2: Trong 93,2 gam E thì nX=ka, nY=kb
=>mE=ka(14n+30)+kb(14m+60)=93,2
Thế (1) và (2) =>k=5
Trong dung dịch NaOH chứa 1,2 mol NaOH và 176/9 mol H2O
Ancol T có M=32=>T là CH3OH
Z gồm:
CH3OH: 5a
H2O: 10b+176/9
m bình tăng=mCH3OH+mH2O-mH2=>160a+180b+352-0,55.2=377,7 (2)
=>a=0,1; b=0,06 thay vào (1): 0,1n+0,06m=0,86 hay 5n+3m=43. Do n, m≥4 nên n=5 và m=6 thỏa mãn
Vậy:
X: C5H8O2 (0,1 mol);
Y: C6H8O4 (0,06 mol)
%mY=0,06.144/(0,1.100+0,06.144)=46,35%