Cho 22,4 gam bột kim loại M vào dung dịch HCl dư, sau khi phản ứng kết thúc thu được 0,8 gam H2. Kim loại M là
A. Mg.
B. Ca
C. Fe
D. Zn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B.
Số mol H2 là:
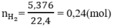
Số mol HCl nHCl = 0,5.1 = 0,5(mol)
2M + 2nHCl → 2MCln + nH2
Số mol HCl phản ứng: nHCl = 2. nH2 = 2.0,24 = 0,48(mol). So với ban đầu HCl phản ứng còn dư
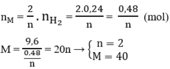
Vậy M là Ca

Số mol khí H2 là:
n(H2) = 5,376/22,4 = 0,24 (mol)
V(ddHCl) = 500ml = 0,5l
Số mol HCl là:
n(HCl) = V(ddHCl).1 = 0,5.1 = 0,5 (mol)
Pthh: 2M + (2x)HCl → 2MClx + (x)H2
Số mol HCl phản ứng:
n(HCl pứ) = 2. n(H2) = 2.0,24 = 0,48 (mol). So với ban đầu thì HCl phản ứng còn dư.
Theo pthh thì: n(M) = 0,48/x (mol)
Khối lượng mol của kim loại M là:
9,6/n(M) = 9,6/(0,48/x) = 20x
--> x = 2 --> 20x = 40 (g/mol)
Vậy M là Ca --> Chọn B.

Chọn B
Gọi hoá trị của kim loại M là n:
2M + 2nHCl → 2MCln + nH2 (1)
=
= 0,24 (mol)
Từ (1) => nM = =
(mol)
Ta có: .M = 96 => M =
Biên luận: n = 1 => M = 20 (loại)
n = 2 => M = 40 (Ca)
n = 3 => M = 60 (loại)

Chọn B
Gọi hoá trị của kim loại M là n:
2M + 2nHCl → 2MCln + nH2 (1)
=
= 0,24 (mol)
Từ (1) => nM = =
(mol)
Ta có: .M = 96 => M =
Biên luận: n = 1 => M = 20 (loại)
n = 2 => M = 40 (Ca)
n = 3 => M = 60 (loại)

a) \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,5}{n}\left(mol\right)\)
Ta có : \(M_M=\dfrac{16,25}{\dfrac{0,5}{n}}=32,5n\)
Chạy nghiệm n
n=1 => M=32,5 (loại)
n=2 => M=65 ( chọn)
n=3 => M=97,5 (loại)
Vậy M là Zn
b) Ta có : \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(lít\right)\)

Đáp án B.
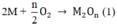
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
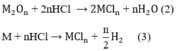
Số mol H2: 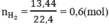
Theo phương trình (1)
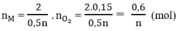
Theo phương trình (3)
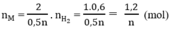
Tổng số mol M là 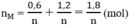
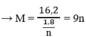
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al

Chọn A.
Ta có: n(H2) = 0,2 → n(Zn) = 0,2 → m(Zn) = 13 (g) → m(Cu) = 2 (g) → m = 2 (g)

Đáp án C
Zn phản ứng vơi HCl tạo H2, kim loại không tan là Cu.
n(H2) = 0,2 mol suy ra n(Zn) =0,2 mol
Nên m(Zn) = 13g
Suy ra m(Cu) = 15- 13= 2g
Đáp án C
Số mol H2 thu được là: n H 2 = 0 , 8 2 = 0 , 4 m o l
Gọi n là hóa trị của M
Phương trình hóa học:
=> M là Fe