Hòa tan hoàn toàn 1,95 gam kim loại K vào H2O thu được 500 ml dung dịch có pH là
A. 13,5
B. 13,0.
C. 14,0.
D. 12,0.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nKOH = nK = 1,95/39 = 0,05 (mol)
=> [KOH] = n :V = 0,05 : 0,5 = 0,1 (M)
=> pH = 14 + lg[OH-] = 14 -1 = 13

Chọn B
Vì: nKOH = nK = 1,95/39 = 0,05 (mol)
=> [KOH] = n :V = 0,05 : 0,5 = 0,1 (M)
=> pH = 14 + lg[OH-] = 14 -1 = 13

PTHH: \(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_K=\dfrac{1,95}{39}=0,05\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{KOH}=0,05\left(mol\right)\\n_{H_2}=0,025\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow C\%=\dfrac{0,05\cdot56}{1,95+12,1-0,025\cdot2}\cdot100\%=20\%\)
\(\Rightarrow\) Chọn B

Đáp án : B
[OH-]B = 0,1 M => nOH(B) = 0,04 mol
=> nOH(A) = nHCl + nOH(B) = 0,14 mol
Vì kim loại chỉ có 1 hóa trị duy nhất => Trong muối clorua thì nOH(trung hòa) = nCl = 0,1 mol
=> chất rắn B gồm : mB = mKL + mOH + mCl
=> mKL = mA = 5,84g

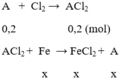
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 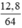 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 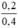 = 0,5M
= 0,5M
Đáp án B
nKOH = nK = 1,95/39 = 0,05 (mol)
=> [KOH] = n :V = 0,05 : 0,5 = 0,1 (M)
=> pH = 14 + lg[OH-] = 14 -1 = 13