thể tích koh 10% có khối lượng riêng 1,12g/ml cần dùng để trung hòa 0,2 mol dung dịch axit h2so4 là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nH2SO4=0.75(mol)
H2SO4+2KOH->K2SO4+2H2O
nKOH=2 nH2SO4->nKOH=1.5(mol)
mKOH=84(g)
mdd=84*100:25=336(g)
H2SO4+2NaOH->Na2SO4+2H2O
nNaOH=1.5(mol) ->mNaOH=60(g)
mdd NaOH=60*100:15=400(g)
V NaOH=400:1.05=381(ml)
Bạn xem lại xem 100 ml hay 1000 ml nhé ^^ tại mình thấy số mol hơi lớn

1. \(n_{Na_2O}=\dfrac{15,5}{62}=0,25\left(mol\right)\)
PTHH: Na2O + H2O → 2NaOH
Mol: 0,25 0,5
\(C_{M_{ddNaOH}}=\dfrac{0,5}{0,5}=1M\)
2.
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,5 0,25
\(m_{ddH_2SO_4}=\dfrac{0,25.98.100}{20}=122,5\left(g\right)\)
\(V_{ddH_2SO_4}=\dfrac{122,5}{1,14}=107,456\left(ml\right)\)
\(n_{Na2O}=\dfrac{m_{Na2O}}{M_{Na2O}}=0,25\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,25 mol - 0,25 mol - 0,5 mol
a) \(C_{M_{NaOH}}=\dfrac{n_{NaOH}}{V_{NaOH}}=1\left(M\right)\)
b) \(H_2SO_4+2NaOH\rightarrow Na_2SO4+2H_2O\)
0,25 mol - 0,5 mol - 0,25 mol - 0,5 mol
\(m_{ctH2SO4}=n_{H2SO4}.M_{H2SO4}=24,5\left(g\right)\)
\(C_{\%_{H2SO4}}=\dfrac{m_{ctH2SO4}}{m_{ddH2SO4}}.100\%\)
\(\Rightarrow m_{ddH2SO4}=\dfrac{m_{ctH2SO4}.100\%}{C_{\%_{H2SO4}}}=122,5\left(g\right)\)
\(D_{H2SO4}=\dfrac{m_{ddH2SO4}}{V_{H2SO4}}\Rightarrow V_{H2SO4}=\dfrac{m_{ddH2SO4}}{D_{H2SO4}}\approx107,46\left(ml\right)\)

a) $2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
b)
n H2SO4 = 0,03.1 = 0,03(mol)
n NaOH = 2n H2SO4 = 0,06(mol)
=> CM NaOH = 0,06/0,05 = 1,2M
c) $H_2SO_4 + 2KOH \to K_2SO_4 + 2H_2O$
n KOH = 2n H2SO4 = 0,06(mol)
=> m KOH = 0,06.56 = 3,36 gam
=> m dd KOH = 3,36/5,6% = 60(gam)
=> V dd KOH = m/D = 60/1,045 = 57,42(ml)

* Phần tính toán:
Khối lượng dung dịch NaOH: m d d = D.V = 1,1.2000=2200(g)
Khối lượng NaOH có trong 2 lit dung dịch:
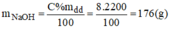
Gọi x(ml) là thể tích của dung dịch NaOH 3% ⇒ m d d = V.d = 1,05.x
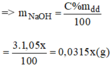
Gọi y(ml) là thể tích của dung dịch NaOH 10% ⇒ m d d = V.d = 1,12.y
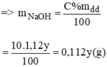
Ta có hệ phương trình sau: 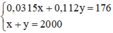
Giải hệ phương trình trên, ta được: 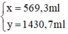
* Cách pha chế:
Đong lấy 569,3ml dung dịch NaOH 3% và 1430,7ml dung dịch NaOH 10% vào bình có dung dịch khoảng 3 lit. Trộn đều ta được 2 lit dung dịch NaOH 8% có khối lượng riêng 1,1g/ml.

PTHH: \(H_2SO_4+2KOH\rightarrow K_2SO+2H_2O\)
Ta có: \(n_{H_2SO_4}=0,2\cdot1=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{KOH}=0,4\left(mol\right)\\n_{K_2SO_4}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{ddKOH}=\dfrac{\dfrac{0,4\cdot56}{6\%}}{1,048}\approx356,2\left(ml\right)\\C_{M_{K_2SO_4}}=\dfrac{0,2}{0,2+0,3562}\approx0,36\left(M\right)\end{matrix}\right.\)
\(n_{H_2SO_4}=1.0,2=0,2\left(mol\right)\\ H_2SO_4+2KOH\rightarrow K_2SO_4+2H_2O\\ 0,2.........0,4........0,2.......0,2\left(mol\right)\\ a.m_{ddKOH}=\dfrac{0,4.56.100}{6}=\dfrac{1120}{3}\left(g\right)\\ V_{ddKOH}=\dfrac{\dfrac{1120}{3}}{1,048}=\dfrac{140000}{393}\left(ml\right)\approx0,356\left(l\right)\)
\(b.C_{MddK_2SO_4}=\dfrac{0,2}{\dfrac{140000}{393}+0,2}\approx0,00056\left(M\right)\)

a. PTPỨ: H2SO4 + 2NaOH \(\rightarrow\) 2H2O + Na2SO4
b. Ta có : nH2SO4 = \(\frac{1.20}{1000}\) = 0,02 mol
c. Theo phương trình: nNaOH = 2.nH2SO4 = 2.0,02 = 0,04 mol
\(\Rightarrow\) mNaOH = 0,04. 40 = 1,6(g)
d. mdd NaOH = \(\frac{1,6.100}{20}\) = 8(g)
e1. PTHH: H2SO4 + 2KOH \(\rightarrow\) K2SO4 + 2H2O
Ta có: nKOH = 2. nH2SO4 = 2. 0,02 = 0,04 mol
\(\Rightarrow\) mKOH = 0,04.56=2,24(g)
e2. mdd KOH = \(\frac{2,24.100}{5,6}\) = 40(g)
e3. Vdd KOH = \(\frac{40}{1,045}\) \(\approx\) 38,278 ml

\(a,PTHH:Na_2O+H_2O\rightarrow2NaOH\\ \Rightarrow n_{NaOH}=2n_{Na_2O}=2\cdot\dfrac{37,2}{62}=0,6\cdot2=1,2\left(mol\right)\\ \Rightarrow C_{M_{NaOH}}=\dfrac{1,2}{0,5}=2,4M\\ b,PTHH:2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\\ \Rightarrow n_{H_2SO_4}=\dfrac{1}{2}n_{NaOH}=0,6\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=0,6\cdot98=58,8\left(g\right)\\ \Rightarrow m_{dd_{H_2SO_4}}=\dfrac{58,8\cdot100\%}{20\%}=294\left(g\right)\\ \Rightarrow V_{dd}=\dfrac{294}{1,14}\approx257,9\left(ml\right)\)

Đổi 300ml = 0,3 lít
Ta có: \(n_{H_2SO_4}=0,3.0,5=0,15\left(mol\right)\)
PTHH: H2SO4 + 2KOH ---> K2SO4 + 2H2O
a. Theo PT: \(n_{KOH}=2.n_{H_2SO_4}=2.0,15=0,3\left(mol\right)\)
\(\Rightarrow V_{dd_{KOH}}=\dfrac{0,3}{0,2}=1,5\left(lít\right)\)
b. Theo PT: \(n_{K_2SO_4}=n_{H_2SO_4}=0,15\left(mol\right)\)
\(\Rightarrow m_{K_2SO_4}=0,15.174=26,1\left(g\right)\)
c. Ta có: \(V_{dd_{K_2SO_4}}=V_{dd_{H_2SO_4}}=0,3\left(lít\right)\)
\(\Rightarrow C_{M_{K_2SO_4}}=\dfrac{0,15}{0,3}=0,5M\)
PTHH: 2KOH + H2SO4 ---> K2SO4 + 2H2O
Theo PT: \(n_{KOH}=2.n_{H_2SO_4}=2.0,2=0,4\left(mol\right)\)
\(\Rightarrow m_{KOH}=0,4.56=22,4\left(g\right)\)
Ta có: \(C_{\%_{KOH}}=\dfrac{22,4}{m_{dd_{KOH}}}.100\%=10\%\)
\(\Rightarrow m_{dd_{KOH}}=224\left(g\right)\)
Theo đề, ta có: \(D=\dfrac{224}{V_{dd_{KOH}}}=1,12\left(\dfrac{g}{ml}\right)\)
\(\Rightarrow V_{dd_{KOH}}=200\left(ml\right)\)