Nguyên tử của nguyên tố R có tổng số hạt p, n, e bằng 18 và tổng số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Vậy số electron độc thân của nguyên tử R là
A. 1
B. 2
C. 3
D. 4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có:
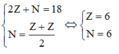
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.
Đáp án D

Đáp án B.
Tổng số các loại hạt proton, nơtron và electron của R là 18
p + n + e = 18 => 2p + n = 18 (1)
Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện
n = (p+e)/2 hay n = p = e (2)
Từ (1), (2) ta có p = e = n =6
Cấu hình e của R : 1s2 2s2 2p2. Số electron độc thân = 2

\(\left\{{}\begin{matrix}P+E+N=18\\P=E\\N=\dfrac{1}{2}\left(P+E\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=18\\P=E=N\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=6\\N=6\end{matrix}\right.\\ \Rightarrow A=Z+N=6+6=12\left(đ.v.C\right)\\ \Rightarrow KH:^{12}_6C\)

\(\left\{{}\begin{matrix}p+e+n=18\\n=\frac{\left(p+e\right)}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p+n=18\\n=\frac{2p}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p+n=18\\n=p\end{matrix}\right.\Leftrightarrow p=e=n=6\)
\(\rightarrow R:C\left(Cacbon\right)\)
Cấu hình: \(1s^22s^22p^2\)
Chọn B
tổng hạt: 2p + n = 18 (1)
Tổng số hạt không mang điện bằng trung bình cộng tổng số hạt mang điện:
\(\Leftrightarrow n=\frac{2p}{2}\Leftrightarrow2n-2p=0\left(2\right)\)
Từ (1) và (2) ta có hpt:
\(\Rightarrow\left\{{}\begin{matrix}2p+n=18\\2n-2p=0\end{matrix}\right.\) \(\Leftrightarrow p=e=n=6\)
Vì p = 6 nên cấu hình của nguyên tử R là:
\(1s^22s^22p^2\)
Vậy số electron độc thân của R là 2 ( chọn câu b )
( giải thích thêm: Vì \(2s^2\) đã bão hòa )

Ta có; p + e + n = 18
Mà p = e, nên: 2p + n = 18 (1)
Theo đề, ta có: p = n (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}2p+n=18\\p=n\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p+n=18\\p-n=0\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3p=18\\p=n\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=6\\n=6\end{matrix}\right.\)
Vậy X là cacbon (C)
Chọn A
Tổng số các loại hạt proton, nơtron và electron của R là 18
p + n + e = 18 => 2p + n = 18 (1)
Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện
n = (p+e)/2 hay n = p = e (2)
Từ (1), (2) ta có p = e = n =6
Cấu hình e của R: 1s2 2s2 2p2. Số electron độc thân ở trạng thái cơ bản là 2

2) gọi số hạt proton, electron,notron lần lượt là p,e,n, ta có p=e
theo đề ta có hệ \(\begin{cases}2p+n=82\\n=\frac{15}{13}n\end{cases}\)<=> \(\begin{cases}p=26\\n=30\end{cases}\)
=> p=e=26 hạt và n=30 hạt
3) theo đề ta có hệ : \(\begin{cases}2p+n=52\\2p-n=16\end{cases}\)<=> \(\begin{cases}p=17\\n=18\end{cases}\)
vậy số hạt trong X có p=e=17 hạt và n=18 hạt
Bài 2 bó tay
Bài 3:
Ta có tổng số hạt cơ bảlà là 52
==> 2p+n=52(1)
Mà 3 số hạt mang điện nhiều hơn số hạt không mang điện là 16
==> 2p-n=16(2)
Từ1 và 2
==> p,n,e,a=?
Đáp án D
Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có: 2 Z + N = 18 N = Z + Z 2 ⇔ Z = 6 N = 6
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.