Cho từ từ 100 ml dung dịch hỗn hợp gồm N a 2 C O 3 0,2M và K H C O 3 0,1M vào 100 ml dung dịch HCl 0,2M, khuấy đều phản ứng hoàn toàn thu được V ml khí C O 2 (đktc). Giá trị của V là
A. 448,0
B. 268,8
C. 191,2
D. 336,0
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
0 , 03 m o l N a H C O 3 0 , 06 m o l K 2 C O 3 nhỏ từ từ 0 , 02 m o l H C l 0 , 06 m o l K H S O 4
=> 2 muối kiềm sẽ phản ứng theo tỉ lệ mol 1:2
Đặt số mol NaHCO3 phản ứng là x => số mol KCO3 phản ứng là 2x
=> nH+ = 0,02 + 0,06 = x + 2.2x => x = 0,016 mol
=> Sau phản ứng có : 0,014 mol HCO3- ; 0,028 mol CO32- và 0,06 mo SO42-
Khi cho X vào dung dịch chứa : 0,06 mol KOH và 0,15 mol BaCl2
=> nCO3 = 0,014 + 0,028 = 0,042 mol ; nSO4 = 0,06 mol
=> m kết tủa = mBaCO3 + mBaSO4 = 22,254g

Đáp án B
Cho từ từ 0,03 mol NaHCO3 và 0,06 mol K2CO3 vào 0,02 mol HCl và 0,06 mol NaHSO4 thu được dung dịch X


Đáp án D
nK2CO3 = nCO3 2- = 0,15.0,1 = 0,015 mol ; nNaHCO3 = nHCO3- = 0,15.0,2 = 0,03 mol
Do ban đầu H+ rất dư so với muối nên 2 muối đều phản ứng đồng thời
CO32- + 2H+ → CO2 + H2O
HCO3- + H+ → CO2 + H2O
=> nCO3 pứ: nHCO3 pứ = 0,015: 0,03 = 1: 2 = x: 2x
nHCl = 0,2.0,2 = 0,04 mol = 2.x + 1.2x = 4x => x = 0,01 mol
=> nCO2 = x + 2x = 3x = 0,03 mol
=> VCO2 = 0,03.22,4 = 0,672 lít = 672 ml

Đáp án A
Chú ý đổ từ từ muối Na2CO3 và NaHCO3 vào dung dịch H2SO4 thì xảy ra đồng thời các phương trình ( HSO4- coi như chất điện ly hoàn toàn tạo ra SO42- và H+)
2H+ + CO32- → CO2 + H2O (1)
2x------> x
H+ + HCO3- → CO2 + H2O (2)
y -----> y
Ta có 2x+ y = 0,08 mol
Vì phản ứng xảy ra đồng thời nên x: y = nCO32- : nHCO3- = 0,06 : 0,03 = 2:1
Ta có hệ 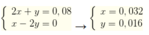
Vậy nCO2 = 0,032 + 0,016 = 0,048 mol → V= 1,0752 l
Vậy dung dịch X chứa : HCO3- dư : 0,014 mol, CO32- :0,028 mol, SO42-:0,06 mol
Khi cho 0,15 mol BaCl2 và 0,06 mol KOH vào dung dịch X xảy ra các pt sau:
HCO3- + OH- → CO32- + H2O
0,014--- 0,06 ----> 0,014
Ba2+ + CO32- → BaCO3↓
0,15 ----0,042 ----> 0,042
SO42- + Ba2+ → BaSO4↓
0,06---------------> 0,06
Vậy mkết tủa = 0,06×233+ 0,042×197 = 22,254 gam

Chọn đáp án C
Tổng nH+ = 0,02 + 0,06 = 0,08 mà có n H C O 3 - = 0,03 và n H C O 3 2 - = 0,06 Þ Tỉ lệ 1: 2
Đặt số mol n H C O 3 - phản ứng = x Þ n H C O 3 2 - phản ứng = 2x Þ x + 2.2x = 0,08
Þ x = 0,08/5 = 0,016
Þ nCO2 = x + 2x = 3x0,016 = 0,048 Þ V = 0,048x22,4 = 1,0752
X lúc này có n S O 4 2 - = 0,06, n B a 2 + = 0,03 - 0,016 = 0,014; n C O 3 2 - = 0,06 - 0,032 = 0,028
Thêm vào X hỗn hợp 0,06 OH- và 0,15 Ba2+ Þ nOH- > n H C O 3 -
Þ Sau phản ứng với OH-, tổng n B a 2 + = 0,014 + 0,028 = 0,042
Vì 0,042 + 0,06 <0,15 Þ Ba2+ dư Þ nBaCO3 = 0,042 và nBaSO4 = 0,06
Vậy m = 0,042x197 + 0,06x233 = 22,254

Đáp án C
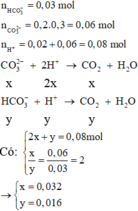
=> V=22,4.(x+y)=1,0752 lít
Dung dịch X chứa 0,028 mol CO 3 2 - , 0,014 mol HCO 3 - , 0,06 mol SO 4 2 - , Na + , K +
Thêm: n OH - = 0 , 06 mol , n Ba 2 + = 0 , 15 mol vào dung dịch X.
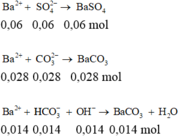
Sau phản ứng dư Ba2+, OH-
n kết tủa = 197 . ( 0 , 028 + 0 , 014 ) + 233 . 0 , 06 = 22 , 254 gam