Một mẫu nước mưa có pH = 4,82. Môi trường của mẫu nước đó là:
A. trung tính.
B. bazơ.
C. axit.
D. không xác định được.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
pH = 4,82 < 7 ⇒ mẫu nước mưa có môi trường axit ⇒ Chọn C

\(n_{NaOH}=\dfrac{8}{40}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\)\(mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,2 0,2
Dung dịch thu được là \(Na_2SO_4\) có môi trường trung hòa.

- Đáp án C
- Từ [OH-]= 1,5.10-5 (M) suy ra:
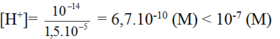
Vậy môi trường của dung dịch là kiềm.

Có [OH-] = 10-5
=> pH = 14 - 5 = 9 > 7
=> Môi trường dung dịch là kiềm
=>D
Đáp án C
pH = 4,82 < 7 ⇒ mẫu nước mưa có môi trường axit ⇒ Chọn C