Dung dịch Ba(OH)2 0,005M có pH bằng
A. 3
B. 2
C. 11
D. 12
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án D
CM Ba(OH)2 = 0,005M ⇒ CM OH– = 0,005 × 2 = 0,01M
⇒ pOH = 2 ⇒ pH = 14 – 2 = 12 ⇒ Chọn D

Chọn đáp án D
CM Ba(OH)2 = 0,005M ⇒ CM OH– = 0,005 × 2 = 0,01M
⇒ pOH = 2 ⇒ pH = 14 – 2 = 12

NaOH và KOH: \(pOH=2,3\Rightarrow pH=11,7\)
\(Ba\left(OH\right)_2:\) \(\left[OH^-\right]=0,005\cdot2=0,01M\)
\(pOH=2\Rightarrow pH=12\)

\(Ba\left(OH\right)_2\rightarrow Ba^{2+}+2OH^-\)
0,005 ________________0,01 (M)
\(\Rightarrow\left[OH^-\right]=0,01M\)
\(\Rightarrow\left[H^+\right]=\frac{10^{-14}}{0,01}=10^{-12}M\)
\(\Rightarrow pH=12\)
Dung dịch làm quỳ tím chuyển xanh.
Bạn tham khảo nhé!

Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 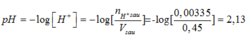
Chọn đáp án D
CM Ba(OH)2 = 0,005M ⇒ CM OH– = 0,005 × 2 = 0,01M
⇒ pOH = 2 ⇒ pH = 14 – 2 = 12