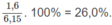Oxi hoá hoàn toàn 6,15 g chất hữu cơ X, người ta thu được 2,25 g H 2 O ; 6,72 lít C O 2 và 0,56 lít N 2 (các thể tích đo ở đktc). Tính phần trăm khối lượng của từng nguyên tố trong chất X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nguyên tố C chiếm 90% và nguyên tố H chiếm 10% về khối lượng.

Câu 7:
\(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Bảo toàn C: nC = 0,6 (mol)
Bảo toàn H: nH = 1,2 (mol)
=> \(n_O=\dfrac{10,8-0,6.12-1,2}{16}=0,15\left(mol\right)\)
=> nC : nH : nO = 0,6 : 1,2 : 0,15 = 4:8:1
=> CTPT: (C4H8O)n
Mà M = 2,25.32 = 72(g/mol)
=> n = 1
=> CTPT: C4H8O
Câu 6
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn C: nC = 0,25 (mol)
Bảo toàn H: nH = 0,6 (mol)
=> \(n_O=\dfrac{4,4-0,25.12-0,6.1}{16}=0,05\left(mol\right)\)
nC : nH : nO = 0,25 : 0,6 : 0,05 = 5:12:1
=> CTPT: (C5H12O)n
Mà M = 44.2=88(g/mol)
=> n = 1
=> CTPT: C5H12O
Câu 8:
MX = 1,875.32 = 60 (g/mol)
Giả sử có 1 mol chất X => mX = 60.1 = 60 (g)
\(m_C=\dfrac{60.40}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{60.6,67}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
\(m_O=60-24-4=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> Trong 1 mol X chứa 2 mol C, 4 mol H, 2 mol O
=> CTPT: C2H4O2

A là hợp chất hữu cơ nên phải chứa cacbon. Oxi hóa A ta được vậy A phải chứa hidro. Theo đầu bài A chỉ chứa hai nguyên tố. Vậy A là hợp chất của cacbon và hidro ( A là một hidrocacbon ).
Khối lượng H trong 3.6g: 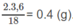
Phần trăm khối lượng của hiđro trong A:
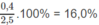
Phần trăm khối lượng của cacbon trong A: 100,0% - 16,0% = 84,0%

Ơ kìa,đang luỵn tập mà. Hay lè giúp tính xắc xuất ik =)))
\(n_{CO_2}=\dfrac{V_{CO_2\left(đktc\right)}}{22,4}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ \Rightarrow n_C=n_{CO_2}=0,03\left(mol\right)\)
\(n_{H_2O}=\dfrac{m}{M}=\dfrac{0,72}{18}=0,04\left(mol\right)\\ \Rightarrow n_{H_2}=2.n_{H_2O}=2.0,04=0,08\left(mol\right)\)
\(\%m_C=\dfrac{m_C}{0,6}=\dfrac{n.M}{0,6}=\dfrac{0,03.12}{0,6}=60\%\\ \%m_H=\dfrac{m_H}{0,6}=\dfrac{n.M}{0,6}=\dfrac{0,08.1}{0,6}=13,33\%\\ \%m_O=100\%-\%m_C-\%m_O=100\%-60\%-13,33\%=26,67\%\)

- Ancol isopropylic: CH 3 2 CHOH là ancol bậc 2 → X là CH 3 – CO – CH 3 (đimetyl xeton).
- Chọn đáp án C.
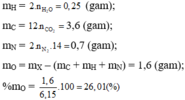
Chất X chắc chắn có C, H, N ; có thể có O.
Khối lượng C: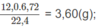
Khối lượng H: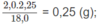
Khối lượng N: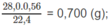
Khối lượng O: 6,15 - 3,60 - 0,25 - 0,700 = 1,60 (g).
% về khối lượng của C: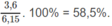
% về khối lượng của H: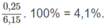
% về khối lượng của N: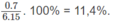
% về khối lượng của O: