Dung dịch Y chứa Ba 2 + 0,05 mol ; Mg 2 + 0,15 mol; Cl - 0,2 mol; HCO 3 - y mol. Đun nóng đến cạn dung dịch Y thu được muối khan có khối lượng là
A. 24,9 gam.
B. 22,7 gam.
C. 18,7 gam.
D. 23,55 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo định luật bảo toàn điện tích có:

Nên tổng khối lượng kết tủa thu được lớn nhất gồm 0,02 mol Mg(OH)2, 0,01 mol Al(OH)3 và 0,02 mol BaSO4
Đáp án B

Đáp án D
CO2 + 2OH- → CO32- + H2O
0,2
CO2 + CO32- + H2O → 2HCO3-
0,05
Ba2+ + CO32- → BaCO3
0,05
⇒m dd = m + 0,15.44 – 197.0,05 = (m – 3,25) gam

Chọn D
Gọi thể tich cần tìm là V lit
,nH+ = nOH- => nHCl + 2nH2SO4 = nNaOH + 2nBa(OH)2
=> 0,1V + 2.0,05V = 0,1 + 2.0,15
=> V = 2 lit

Đáp án C
Có dung dịch X gồm NaCl (0,12 mol), và (NH4)2SO4 (0,025 mol)
(NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3 + 2H2O
Sau phản ứng dư: 0,005 mol Ba(OH)2 trong dung dịch
m= 0,12.58,5 + 0,005.171 = 7,875 gam

Đáp án C
+ N a + : 0 , 12 N H 4 + : 0 , 05 C l - : 0 , 12 S O 4 2 - : x = 0 , 025 ⏟ d u n g d ị c h X + B a 2 + : 0 , 03 O H - : 0 , 06 l → B a S O 4 : 0 , 025 N H 3 : 0 , 05 + N a + : 0 , 12 l C l - : 0 , 12 B a 2 + : 0 , 005 O H - : 0 , 01 ⏟ d u n g d ị c h Y + Y → c ô c ạ n m c h ấ t r ắ n = m i o n = 7 , 875 g a m

Đáp án A
Bảo toàn điện tích suy ra x = 0,025 mol
Ba2++ SO42-→BaSO4
0,03 0,025 0,025
OH-+ NH+4→ NH3+ H2O
0,06 0,05
Dung dịch Y có 0,12 mol Na+; 0,12 mol Cl-; 0,005 mol Ba2+; OH- 0,01 mol
Khi cô cạn thu được m = 0,12.23+ 0,12.35,5+ 0,005.137+ 0,01.17 = 7,875 gam

Theo BTĐT: x = (0,12 + 0,05 – 0,12) : 2 = 0,025 mol.
Cho 0,03 mol Ba(OH)2 phản ứng với ddX
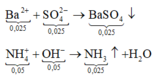
Vậy khi phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa thu được ddY gồm 0,12 mol Na+; 0,12 mol Cl−; 0,005 mol Ba2+; 0,01 mol OH−
Vậy m = 0,12x23 + 0,12x35,5 + 0,005x137 + 0,01x17 = 7,875 gam
Đáp án A
Chọn D
Bảo toàn điện tích: 2.0,05 + 2.0,15 = 0,2 + y → y = 0,2 mol
Đun nóng Y:
Khối lượng muối khan: 0,05.137 + 0,15.24 + 0,2.35,5 + 0,1.60 = 23,55 gam.