Cho a mol Ba(OH)2 vào dung dịch chứa b mol NaHCO3 (biết a < b < 2a). Sau khi kết thúc tất cả phản ứng thu được kết tủa X và dung dịch Y. Số chất tan trong Y là
A. 1
B. 2
C. 3
D. 4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D
TN1 và TN2 → Khi dùng BaCl2 dư thì thu được kết tủa gấp 2 lần dùng KOH dư.
Dãy chất: Ba(HCO3)2, Al(NO3)3, K2CO3: TN1 cho 1 mol kết tủa, TN2 cho 1 mol kết tủa.
Dãy chất: AlCl3, FeSO4, Ba(HCO3)2: TN1 cho 3 mol kết tủa, TN2cho 2 mol kết tủa.
Dãy chất: Ca(HCO3)2, Ba(NO3)2, Al2(SO4)3: TN1 cho 1 mol kết tủa, TN2 cho 3 mol kết tủa

Chọn C.
Các chất trong X lần lượt là 1, 2, 3 mol. Các phản ứng xảy ra:
OH- + HCO3- ® CO32- + H2O
Ca2+, Ba2+ + CO32- ® CaCO3, BaCO3
Nếu các chất đó là Al(NO3)3, Ca(HCO3)2, Ba(HCO3)2 Þ a = 5; b = 10 và c = 5
Nếu các chất đó là Ba(HCO3)2, Ba(NO3)2, Ca(HCO3)2 Þ a = 4; b = 8 và c = 4
Nếu các chất đó là Ca(HCO3)2, Fe(NO3)2, Al(NO3)3 Þ a = 3; b = 4 và c = 1 (thoả mãn)
Nếu các chất đó là Ca(HCO3)2, Ba(NO3)2, Al(NO3)3 Þ a = 1; b = 2 và c = 1

Đáp án : A
Bảo toàn điện tích : nH+ + 3nAl3+ = nNO3- + 2nSO4 => 3a – b = -0,06
, nOH = nKOH + 2nBa(OH)2 = 0,168 mol ; nBa2+ = 0,012 mol
, mkết tủa = mBaSO4 + mAl(OH)3 => nAl(OH)3 = 0,012 mol < 1/3( nOH – nH+)
=> Có hiện tượng kết tủa tan 1 phần => nAl(OH)3 = 4nAl3+ - (nOH- - nH+)
=> nAl3+ = a = 0,02 => b = 0,12
Đáp án B
n O H - = 2 a
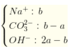
Do b < 2a nên lượng HCO3- phản ứng hết với OH- (OH- vẫn còn dư) tạo CO3 2-.
a < b nên Ba2+ bị kết tủa hết bởi CO3 2- (CO3 2- vẫn còn dư)
Như vậy, trong Y có
Vậy, trong Y có 2 chất tan