Sục V lít khí CO2 (đktc) vào 2 lít dung dịch Ca(OH)2 0,05M , thu được 7,5 gam kết tủa . Gía trị V là
A. 1,68 lít
B. 2,88 lít
C. 2,24 lít và 2,8 lít
D. 1,68 lít và 2,8 lít
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
CaO+ H2O → Ca(OH)2
Ta có: nCa(OH)2= nCaO= 0,05 mol; nCO2= 1,68/22,4= 0,075 mol
Khi sục khí CO2 vào dung dịch A:
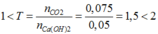
→ Tạo 2 muối
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2+ Ca(OH)2 → Ca(HCO3)2 (2)
Ca(HCO3)2→ CaCO3+ CO2+ H2O (3)
Đặt số mol CaCO3 PT 1 là x mol; số mol Ca(HCO3)2 PT 2 là y mol
Ta có: nCO2= x+2y= 0,075 mol; nCa(OH)2= x+y= 0,05 mol
→x=y= 0,025 mol→ m= mCaCO3= 0,025.100= 2,5 gam
Theo PT (2) và (3): nCaCO3= nCa(HCO3)2= 0,025 mol
→m'= mCaCO3= 0,025.100= 2,5 gam

nCa(OH)2= 0,2.1 = 0,2 mol.
nCaCO3 = 15 : 100 = 0,15mol
Cho NaOH vào dung dịch sau PƯ thấy xuất hiện kết tủa nên trong dd có muối Ca(HCO3)2
Vậy xảy ra 2 phản ứng:
CO2 + Ca(OH)2 -----> CaCO3 + H2O (1)
0,15 mol 0,15 mol 0,15 mol
2CO2 + Ca(OH)2 ------> Ca(HCO3)2 (2)
2. 0,05 mol 0,05 mol
Theo (1) : nCO2(1) = nCa(OH)2 (1) = nCaCO3 = 0,15mol
=> nCa(OH)2 (2) = 0,2 - 0,15 = 0,05 mol
Theo (2) : nCO2 (2) = 2. 0,05 = 0,1 mol
=> nCO2 = 0,15 + 0,1 = 0,25 mol
=> VCO2 = 0,25 . 22,4 = 5,6 (L)
nCaCO3 = 10 / 100 = 0,1 chứ ạ !!
vì m kết tủa bằng 10 chứ ạ ???? giải thích hộ vs ạ

Đáp án D
Lượng CO 2 tham gia phản ứng và lượng Ba ( OH ) 2 ở hai thí nghiệm đều bằng nhau, nhưng ở TN1 thu được lượng kết tủa ít hơn ở TN2. Suy ra ở TN1 kết tủa đã bị hòa tan một phần. Dựa vào tính chất của đồ thị ở TN1 suy ra :
n CO 2 = 2 n Ba ( OH ) 2 - n BaCO 3 = ( 2 a - 0 , 1 ) mol
Đồ thị biểu diễn sự biến thiên lượng kết tủa theo lượng CO 2 ở TN1 và TN2 :
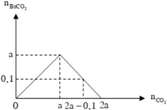
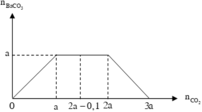
Dựa vào 2 đồ thị, ta thấy a < 2a - 0,1 < 2a nên ở TN2 kết tủa đạt cực đại. Suy ra :
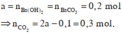
Vậy V = 6,72 lít và a = 0,2 mol

Đáp án B
Ta có: n B a ( O H ) 2 = 0,12 mol; n C O 2 = 0,1 mol ; n C O 2 = 0,2 mol
-Tại điểm cực đại:
CO2+ Ba(OH)2 → BaCO3+ H2O
0,12 0,12 0,12
Vậy khi n C O 2 = 0,12 mol thì lượng kết tủa đạt cực đại
Vậy khi đi từ n C O 2 = 0,1 mol đến 0,12 mol thì lượng kết tủa sẽ dần tăng lên. Khi đi từ n C O 2 = 0,12mol đến 0,2 mol thì lượng kết tủa sẽ dần giảm xuống
→Lượng kết tủa nhỏ nhất khi n C O 2 = 0,1 mol hoặc 0,2 mol.
-Khi n C O 2 = 0,1 mol
CO2+ Ba(OH)2 → BaCO3+ H2O
0,10 0,10 0,10 mol
Ta có: n B a C O 3 = 0,1 mol
-Khi n C O 2 = 0,2 mol
CO2+ Ba(OH)2 → BaCO3+ H2O
x x x mol
2CO2 + Ba(OH)2 → Ba(HCO3)2
2y y mol
Ta có: n B a ( O H ) 2 = x + y = 0,12 mol ; n C O 2 = x+ 2y = 0,2 mol
→ x = 0,04 mol ; y = 0,08 mol
Ta có: n B a C O 3 = 0,04 mol
So sánh 2 trường hợp trên ta thấy n B a C O 3 m i n = 0,04 mol → m B a C O 3 m i n = 7,88 gam

Đáp án : D
Ta có :
n Ca(OH)2 = 0,0125 mol ;
n NaOH 0,025 mol ;
n CO2 = 0,03 mol
=> n Ca2+ = 0 ,0125 mol
=> n OH- = 0,05 mol
Ta thấy :
1 < nOH- / nCO2 = 0,05/ 0,03 = 1,67 < 2
=> khi cho CO2 vào hỗn hợp 2 bazơ phản ưng tạo ra 1 ion HCO3- và CO32-
CO2 + 2OH- → CO32- + H2O (1)
x 2x x
CO2 + OH- → HCO3- (2)
y y y
ta có :
x + y = 0,03 (4)
2x + y = 0,05 (5)
Từ (4) (5) ta được x = 0,02 ; y = 0,01
Phản ứng tạo kết tủa
Ca2+ + CO32- → CaCO3
0,0125 0,0125
=> m kết tủa = 0,0125.100 = 1,25g
=> Đáp án D
* Cách khác
Ta có :
n CO32- = nOH- - nCO2 = 0,05 – 0,03 = 0,02 mol
phản ứng :
Ca2+ + CO32- → CaCO3
0,0125 0,0125
m ↓ = 0,0125 . 100 = 1,25g
Đáp án : D
Ta có : n CaCO3 = 7,5 /100 = 0,075 mol
n Ca(OH)2 = 0,1 mol
ta thấy : nCaCO3 ≠ nCa(OH)2 => có 2 trường hợp
TH1 : chỉ xảy ra phản ứng tạo CaCO3 và Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
=> VCO2 = 0,075.22,4 = 1,68 lít
TH2 : xảy ra 2 phản ứng tạo muối CaCO3và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 0,025
=> tổng nCO2 = 0,075 + 0,05 = 0,125 mol
=> VCO2 = 0,125.22,4 = 2,8 lít
=> Đáp án D
CÁCH KHAC : Sử dụng phương pháp đồ thị
Dựa vào đồ thị => n CO2 = 0,075 mol hoặc n CO2 = 0,125 mol
=> VCO2 = 0,075.22,4 =1,68 lít hoặc VCO2 = 0,125.22,4 = 2,8 lít