Để luyện được 500 tấn thép cacbon (thành phần gồm Fe và C) chứa 1,4% C, cần dùng x tấn quặng hematit đỏ chứa 0% tạp chất trơ. Hiệu suất quá trình là 75%. Giá trị của x là
A. 939,05.
B. 528,21.
C. 1878,10.
D. 1056,43.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

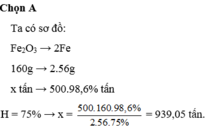

Ta có sơ đồ:
Fe 2 O 3 → 2 Fe
160g → 2.56g
x tấn → 500.98,6% tấn
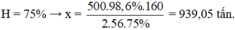
Chọn đáp án A.

Chọn A
Ta có sơ đồ:
F e 2 O 3 → 2 F e
160g → 2.56g
x tấn → 500.98,6% tấn
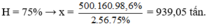

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
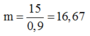

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.


m Fe3O4 = 80 tấn
=> n Fe = 1,03 (tấn mol)
=> m gang theo lý thuyết = 60,98 tấn
=> m gang thực tế = 60,98.93% = 56,71 tấn
=>D

Ta có: mFe = 2.90% = 1,8 (tấn) = 1800000 (g)
\(\Rightarrow n_{Fe}=\dfrac{1800000}{56}=\dfrac{225000}{7}\left(mol\right)\)
BTNT Fe, có: nFe2O3 = 1/2nFe = 112500/7 (mol)
\(\Rightarrow m_{Fe_2O_3}=\dfrac{112500}{7}.160=\dfrac{18000000}{7}\left(g\right)=\dfrac{18}{7}\left(tan\right)\)
Vì: H% = 80% ⇒ mFe2O3 (thực tế) = 18/7:80% = 45/14 (tấn)
Mà: Quặng hematit chứa 60% Fe2O3
⇒ mquặng = 45/14:60% ≃ 5,36 (tấn)

\(m_{Fe_2O_3}=12000.85\%=10200(kg)\\ \Rightarrow n_{Fe_2O_3}=\dfrac{10200}{160}=63,75(kmol)\\ \Rightarrow n_{Fe_2O_3(p/ứ)}=63,75.80\%=51(kmol)\\ \Rightarrow n_{Fe}=2n_{Fe_2O_3}=102(kmol)\\ \Rightarrow m_{Fe}=102.56=5712(kg)\\ \Rightarrow m_{gang}=\dfrac{5712}{96\%}=5950(kg)=5,95(tấn)\)