Cho 5,6 g sắt tác dụng với dung dịch axit clohidric loãng thu được bao nhiêu ml khí H 2
A. 2,24 ml
B. 22,4 ml
C. 2240 ml
D. 0,0224 ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. B
2. B
(Câu 2 cậu nên sửa lại câu hỏi nhé: Khối lượng dung dịch NaOH 10% ...)
Câu 1.
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\)
Chọn B.
Câu 2. \(n_{HCl}=0,2\cdot1=0,2mol\)
Để trung hòa: \(\Rightarrow n_{H^+}=n_{OH^-}=0,2\)
\(m_{NaOH}=0,2\cdot40=8\left(g\right)\)
\(m_{ddNaOH}=\dfrac{8}{10\%}\cdot100\%=80\left(g\right)\)
Chọn B.

Câu 2 :
$a) Mg + 2HCl \to MgCl_2 + H_2$
$n_{HCl} = 0,2.1 = 0,2(mol)$
Theo PTHH : $n_{H_2} = n_{MgCl_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
$b) m_{MgCl_2} = 0,1.95 = 9,5(gam)$
Câu 3 :
a) $Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH :
$n_{H_2SO_4} = n_{H_2} = n_{Fe} = \dfrac{5,6}{56} = 0,1(mol)$
$C\%_{H_2SO_4} = \dfrac{0,1.98}{500}.100\% = 1,96\%$
b)
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
c)
$2H_2 + O_2 \xrightarrow{t^o} 2H_2o$
$V_{O_2} = \dfrac{1}{2}V_{H_2} = 1,12(lít)$

2Fe+ 3Cl2=(t0) 2FeCl3
nFeCl3=16,25/162,5=0,1 mol => nCl2=3/2nFeCl3=3/2.0,1=0,15 mol
2KMnO4+ 16HCl=2KCl+2MnCl2+5Cl2+8H2O
nKMnO4=2/5.nCl2=2/5. 0,15=0,06 mol --> mKMnO4=0.06. 158=9,48 g
nHCl=16/5. nCl2=16/5. 0,15=0,48 mol
--> VddHCl=0,48/ 1=0,48 lit= 480 ml

\(n_{Fe}=\dfrac{5,6}{56}=0,1(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=0,1(mol)\\ \Rightarrow V_{H_2(đkc)}=0,1.24,79=2,479(l)=2479(ml)\)
Chọn B

cậu xem lại đề bài được không tính m nhưng mình không thấy m ở phần trên phần cuối lại độp phat tính m

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
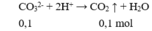
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
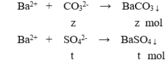
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
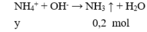
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.
Đáp án C
F e + 2 H C l → F e C l 2 + H 2 N h ì n v à o p h ư ơ n g t r ì n h t h ấ y n F e = n H 2 = 5 , 6 / 56 = 0 , 1 m o l V H 2 = 0 , 1 . 22 , 4 = 2 , 24 l = 2240 m l