Cho biết 1 mol chất khí ở điều kiện bình thường có thể tích là
A. 2,24 l
B. 0,224 l
C. 22,4 l
D. 22,4 ml
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Zn+2HCl->Zncl2+H2
0,1-------------------0,1
n Zn=0,1 mol
=>VH2=0,1.22,4=2,24l
=>C

Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic:
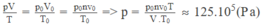


Ở cùng điều kiện về nhiệt độ và áp suất, một mol bất kì chất khí nào cũng có thể tích là
A. 22,2 lít. B. 22 lít.
C. 22,4 lít. D. 24,2 lít.

\(n_{SO_2}=\dfrac{12.10^{23}}{6.10^{23}}=2mol\)
\(V_{SO_2}=2.22,4=44,8l\)
=> Đáp án D

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=0,2.1=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,2}{2}\) => HCl hết, Fe dư
PTHH: Fe + 2HCl --> FeCl2 + H2
__________0,2---------------->0,1
=> VH2 = 0,1.22,4 = 2,24(l)
=> B

Chọn B vì thể tích còn phải tùy thuộc vào áp suất và nhiệt độ, phải cùng nhiệt độ và áp suất mới có thể tích bằng nhau
Đáp án C