Thế nào là phản ứng oxi hoá – khử? Lấy ví dụ minh hoạ.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

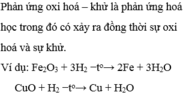

sự oxi hóa là phản ứng giữa Oxi với 1 chất
phản ứng hóa hợp là phản ứng chỉ có 1 chất mới được tạo thành từ 2 hay nhiều chất ban đầu
VD : S+O2 -to-> SO2
phản ứng phân hủy là phản ứng chỉ có 1 chất ban đầu tạo thành 2 hoặc nhiều chất sản phẩm
VD : 2KMnO4 -to-> K2MnO4 + MnO2 +O2
phản ứng thế là phản ứng 2 giữa đơn chất và hợp chất , nguyên tử của đơn chất sẽ thay thế nguyên tử 1 nguyên tố khác trong hợp chất
VD : Zn + 2HCl -> ZnCl2 + H2

Câu 1: Phản ứng oxi hoá – khử là phản ứng hoá học trong đó có xảy ra đồng thời sự oxi hoá và sự khử.
Ví dụ: Fe2O3 + 3H2 −to→ 2Fe + 3H2O
CuO + H2 −to→ Cu + H2O
Phản ứng oxi hoá – khử là phản ứng hoá học trong đó có xảy ra đồng thời sự oxi hoá và sự khử.
Ví dụ: Fe2O3 + 3H2 −to→ 2Fe + 3H2O
CuO + H2 −to→ Cu + H2O

Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự chuyển electron giữa các chất phản ứng.
Thí dụ:
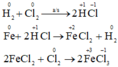

ClO - và ClO 3 - có cấu tạo tương ứng như sau :
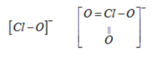
Liên kết ClO - trong ClO 3 - ngắn hơn trong ClO - nên độ bền ClO 3 - > ClO - Do đó tính oxi hoá ClO 3 - < ClO -
Trong dung dịch nước, ion ClO 3 - chỉ oxi hoá trong môi trường axit mạnh, còn ion ClO - oxi hoá trong bất kì môi trường nào.
NaClO + 2KI + H 2 O → NaCl + I 2 + 2KOH
NaCl O 3 + 6KI + 3 H 2 SO 4 → NaCl + 3 I 2 + 3 K 2 SO 4 + 3 H 2 O

Các chất có thể đóng vai trò chất oxi hoá là S, SO 2 , H 2 SO 3 . Thí dụ
a) S + 2Na → Na 2 S
b) SO 2 + 2 H 2 S → 3S + 2 H 2 O
c) H 2 SO 3 + 2 H 2 S → t ° 3S + 3 H 2 O
Các chất có thể đóng vai trò chất khử là S, H 2 S , SO 2 , H 2 SO 3 . Thí dụ
a) S + O 2 → t ° SO 2
b) H 2 S + Cl 2 → S + 2HCl
c) SO 2 + Br 2 + 2 H 2 O → H 2 SO 4 + 2HBr
d) 5 H 2 SO 3 + 2 KMnO 4 → 2 H 2 SO 4 + K 2 SO 4 + 2Mn SO 4 + 3 H 2 O

SO 2 2 SO 2 + 2 H 2 O + O 2 → 2 H 2 SO 4 2 H 2 S + SO 2 → 2 H 2 O + 3 S

HCl 2 HCl + Fe → FeCl 2 + H 2 4 HCl + MnO 2 → MnCl 2 + Cl 2 + 2 H 2 O

Cu Br 2
Cu Br 2 là chất oxi hóa
Cu Br 2 + Fe → Fe Br 2 + Cu
Cu Br 2 là chất khử
Cu Br 2 + Cl 2 → Cu Cl 2 + Br 2