Phần trăm về khối lượng của nguyên tố nitơ trong hiđroxit ứng với oxit cao nhất có giá trị gần nhất với giá trị nào sau đây?
A. 14,89%. B. 22,58%. C. 36,84%. D. 25,93%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTHH của X : $R_2O$
Ta có : $\%R = \dfrac{2R}{2R + 16}.100\% = 74,194\% \Rightarrow R = 23(Natri)$
$Na_2O + H_2O \to 2NaOH$
$m_{dd\ Y} = 15,5 + 184,5 = 200(gam)$
$n_{NaOH} = 2n_{Na_2O} = 2.\dfrac{15,5}{62} = 0,5(mol)$
$C\%_{NaOH} = \dfrac{0,5.40}{200}.100\% = 10\%$
Chọn đáp án B

Đáp án A
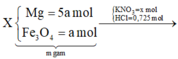
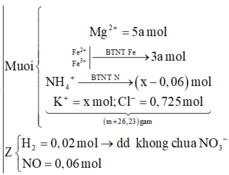
Theo giả thiết, ta có:
![]()
![]()
Khi đó, ta có:
24.5a + 56.3a+ 18x(x-0,06)+ 39x+35,5.0,725 = (325a + 26,23) gam
=> 64a - 57x = -1,5725 gam(I)
Mặt khác, khi đề bài cho số mol H + thì ta nghĩ ngay đến mối liên hệ của mol H +
Theo đó,ta có:
![]()
![]()
![]()
![]()
Vậy (1) và (2) có hệ
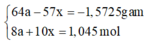
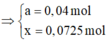
=> %Fe(trong muối)
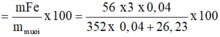
![]()

Viết lại đề bài bạn nhé ! Gì mà "trong cthh oxit không có oxi " ??? Oxit mà làm sao không có oxi được?

Chọn B
R có 4 electron lớp ngoài cùng, e cuối cùng điền vào phân lớp np → R thuộc nhóm IVA
→ Hợp chất khí với hiđro và oxit cao nhất của R lần lượt là R O 2 , R H 4 .
Ta có:
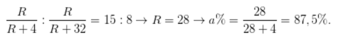

Đáp án A
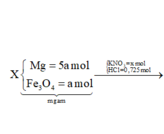
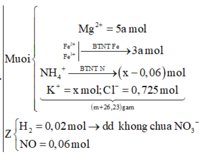
Theo giả thiết, ta có:
![]()
![]()
Khi đó, ta có: 24 x 5a + 56 x 3a + 18 x (x - 0,06) + 39x + 35,5 x 0,725 = (352a + 26,23) gam
![]()
Mặt khác, khi đề bài cho số mol H + thì ta nghĩ ngay đến mối liên hệ của mol H +
Theo đó,ta có: ![]()
=> 0,725 = 2.4a + 2.0,02 + 4.0,06 + 10()x - 0,06
=> 8a + 10x = 1,405 mol (2)
Vậy (1) và (2) có hệ 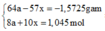
![]()
=> %mFe (trong muối) = 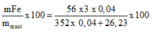
![]()

Đáp án A.
Hợp chất khí với Hidro của R có công thức là RHx ( 4
≥
x
≥
1) => Oxit cao nhất của R là ![]() . Theo đề bài ta có:
. Theo đề bài ta có:

Ta có:
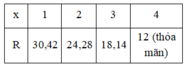
Vậy R là C
=> Hợp chất khí với Hidro là CH4 và Oxit cao nhất là CO2
Nhận xét các đáp án:
A đúng: Do CO2 có cấu trúc mạch thẳng O – C – O nên lực hút của nguyên tử Oxi triệt tiêu lẫn nhau CO2 có liên kết cộng hóa trị giữa nguyên tử C và O phân cực nhưng phân tử CO2 không phân cực.
B sai: Ở điều kiện thường CO2 là hợp chất khí.
C sai: Trong bảng tuần hoàn C thuộc chu kì 2.
D sai: Ở trạng thái cơ bản C có 4 electron s.

