Oxit cao nhất của một nguyên tố ứng với công thức R2O5 (A). Trong hợp chất của nó với hiđro (B), R chiếm 91,18% về khối lượng. Xác định nguyên tố R và các công thức A,B
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


B: RH 3 → % m R = R/R+3 x 100 = 82,35
→ R = 14(N) → A,B là N 2 O 5 và NH 3
Cho em hỏi làm sao mình biết đc R có hoá trị 3 khi tác dụng với hidro ạ.

Oxit cao nhất của R có CTHH là R2O5
=> CTHH hợp chất khí với hidro là RH3
Có: \(\%R=\dfrac{NTK_R}{NTK_R+3}.100\%=91,18\%\)
=> NTKR = 31 (đvC)
=> R là P(Photpho)
CTHH oxit cao nhất: P2O5
CTHH hợp chất khí với hidro: PH3

Bài của Tuệ Lâm hướng đi đúng nhưng ráp số bị sai. Anh hướng dẫn em nha!
---
CT oxit cao nhất: R2O5 (R hoá trị V)
Ta có: hợp chất với H + Hợp chất oxit của R có hoá trị cao nhất sẽ có hoá trị tổng là VIII (8)
-> Hc R với H thì R có hoá trị III => CTHH: RH3
Vì đề bài thì R chứa 91,18% khối lượng. Nên ta được:
\(\%m_R=\dfrac{M_R}{M_R+3}.100\%=91,18\%\\ \Leftrightarrow M_R=31\left(\dfrac{g}{mol}\right)\\ \Rightarrow R:Photpho\left(P=31\right)\\ \Rightarrow CTHH:PH_3\)

Đáp án A
Hướng dẫn Nguyên tố có oxit cao nhất là R2O5 → R thuộc nhóm VA
→ Hợp chất với hidro: RH3
![]() → MR = 14. Đó là nguyên tố N
→ MR = 14. Đó là nguyên tố N

a)
Do R thuộc nhóm VA
=> CTHH của R và H là: RH3
Có \(\dfrac{3}{M_R+3}.100\%=17,64\%=>M_R=14\left(g/mol\right)\)
=> R là N
b) Do CTHH của R và H là RH3
=> oxit cao nhất của R là R2O5
Có: \(\dfrac{16.5}{2.M_R+16.5}.100\%=74,07\%=>M_R=14\left(g/mol\right)\)
=> R là N


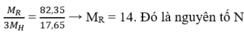
Bạn tham khảo lời giải ở đây nhé!
Câu hỏi của Huong LE - Hóa học lớp 8 | Học trực tuyến
Từ đó suy ra A là N2O5 và B là NH3.