Hoà tan hỗn hợp Ba Na với tỉ lệ mol 1:1 vào H2O được dung dịch A và 0,672l khí ở đktc. Tính thể tích dung dịch HCl 0,1M cần để trung hòa dung dịch A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Bài toán này có thể giải ngắn gọn như sau:
Số mol tạo ra = số mol H+ trung hòa = 2. Số mol H2
⇒ Số mol H2 = 0,075 : 2 = 0,00375 ⇒ V = 0,84 lít

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ Mg+2HCl\to MgCl_2+H_2\\ MgO+2HCl\to MgCl_2+H_2O\\ \Rightarrow n_{Mg}=0,1(mol)\\ \Rightarrow \%_{Mg}=\dfrac{0,1.24}{6,4}.100\%=37,5\%\\ \Rightarrow \%_{MgO}=100\%-37,5\%=62,5\%\)
\(b,n_{MgO}=\dfrac{6,4-0,1.24}{40}=0,1(mol)\\ \Rightarrow n_{HCl}=2.0,1+2.0,1=0,4(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,4}{0,5}=0,8(l)\\ c,n_{MgCl_2}=0,1+0,1=0,2(mol)\\ \Rightarrow C_{M_{MgCl_2}}=\dfrac{0,2}{0,8}=0,25M\)

B1:
Cho dd NaOH vào hỗn hợp thì dd NaOH sẽ phản ứng với HCl trước sau đó mới phản ứng với muối AlCl3
Để kết tủa là cực đại <=> Không có quá trình hoà tan Al(OH)3
\(NaOH+HCl\rightarrow NaCl+H_2O\\ AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\\ n_{NaOH}=n_{HCl}+3.n_{AlCl_3}=0,01+0,02.3=0,07\left(mol\right)\\ \Rightarrow V_{ddNaOH}=\dfrac{n_{NaOH}}{C_{MddNaOH}}=\dfrac{0,07}{0,1}=0,7\left(lít\right)\)
2)
\(n_{Al_2\left(SO_4\right)_3}=0,0001.V\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,0003.V<--0,0001.V------>0,0003.V-->0,0002.V
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
(0,1-0,0006.V)<-(0,05-0,0003.V)
=> 233.0,0003.V + 78.(0,0008.V-0,1) = 12,045
=> V = 150 (ml)
3) \(n_{K_2SO_4.Al_2\left(SO_4\right)_3.24H_2O}=\dfrac{47,4}{948}=0,05\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{K_2SO_4}=0,05\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,15<-------0,05----------->0,15----->0,1
\(Ba\left(OH\right)_2+K_2SO_4\rightarrow BaSO_4+2KOH\)
0,05---------------------->0,05--->0,1
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
0,1--->0,1
=> mkt = mBaSO4 = 0,2.233 = 46,6(g)

Đáp án D
Gọi x, y là số mol của Na2CO3 và K2SO4 trong hỗn hợp.
Phương trình phản ứng xảy ra:
Na2CO3 + 2HCl " 2NaCl + CO2 + H2O (1)
x 2x x
K2SO3 + 2HCl " 2KCl + SO2 + H2O (2)
y 2y y
2HCl + Ba(OH)2 " BaCl2 + 2H2O (3)
0,04 0,02
Theo đề bài ta có: 106x + 158y = 3,9 (I)
Mặt khác: 44 x + 16 y x + y = 33,586.16 => -13,328x + 6,672y = 0 (II)
ð x = 0,00925 mol; y = 0,0185 mol
ð %Na2CO3 = 0 , 00925 . 106 3 , 9 .100% = 25,14 à %K2SO3 = 74,86%

Đáp án D
X + nH2O → X(OH)n + n/2 H2.
Ta có: n H 2 = 0,15 mol → n O H - = 2 n H 2 = 0,3 mol → n H + = 0,3 mol → 2. 2V = 0,3 → V = 0,075 (lít)

Đáp án D
X + nH2O → X(OH)n + n/2 H2.
Ta có: n(H2) = 0,15 mol → n(OH-) = 2n (H2) = 0,3 mol → n(H+) = 0,3 mol → 2. 2V = 0,3 → V = 0,075 (lít)

Chọn B.
Theo đề ta có: n O 2 = 1 , 225 ; n C O 2 = 1 , 05 v à n H 2 O = 1 , 05 => X no, đơn chức, mạch hở (vì n C O 2 = n H 2 O )
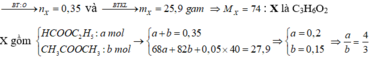
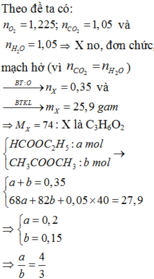
\(n_{H_2}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
_______a--------------------->a---------->a______(mol)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
_a----------------------->a------>0,5a_______(mol)
=> a + 0,5a = 0,03
=> a = 0,02 (mol)
PTHH: \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
________0,02-------->0,04_______________________(mol)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
_0,02----->0,02_______________________(mol)
=> \(n_{HCl}=0,04+0,02=0,06\left(mol\right)\)
=> CM(HCl) = \(\frac{0,06}{0,1}=0,6\left(l\right)\)