Cho 3,94 gam một muối cacbonat của kim loại hóa trị II vào dung dịch HCl dư thu được 0,448 lít CO2(đktc). Vậy kim loại hóa trị II là:
A. Be (M=9)
B. Ca (M=40)
C. Ba (M=137)
D. Mg (M=24)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
• muối cacbonat kim loại hóa trị II: MCO3 + 2HCl → MCl2 +CO2↑ + H2O
• muối cacbonat kim loại hóa trị I: N2CO3 + 2HCl → 2NCl + CO2↑ + H2O
từ tỉ lệ phản ứng có: ∑nHCl = 2∑nCO2↑ = 0,09 mol.
m gam muối khi cô cạn A là muối clorua, là sự thay thế 1 gốc CO32− bằng 2 gốc Cl.
⇒ tăng giảm khối lượng có: m = mmuối clorua = 21 + (0,09 × 35,5 – 0,045 × 60) = 21,495 gam.
⇒ Chọn đáp án C.

• muối cacbonat kim loại hóa trị II: MCO3 + 2HCl → MCl2 +CO2↑ + H2O
• muối cacbonat kim loại hóa trị I: N2CO3 + 2HCl → 2NCl + CO2↑ + H2O
từ tỉ lệ phản ứng có: ∑nHCl = 2∑nCO2↑ = 0,09 mol.
m gam muối khi cô cạn A là muối clorua, là sự thay thế 1 gốc CO32- bằng 2 gốc Cl.
⇒ tăng giảm khối lượng có: m = mmuối clorua = 21 + (0,09 × 35,5 – 0,045 × 60) = 21,495 gam
Đáp án C

Chọn đáp án C
• muối cacbonat kim loại hóa trị II: MCO3 + 2HCl → MCl2 +CO2↑ + H2O
• muối cacbonat kim loại hóa trị I: N2CO3 + 2HCl → 2NCl + CO2↑ + H2O
từ tỉ lệ phản ứng có: ∑nHCl = 2∑nCO2↑ = 0,09 mol.
m gam muối khi cô cạn A là muối clorua, là sự thay thế 1 gốc CO32- bằng 2 gốc Cl.
⇒ tăng giảm khối lượng có: m = mmuối clorua = 21 + (0,09 × 35,5 – 0,045 × 60) = 21,495 gam.
⇒ Chọn đáp án C
21 + (0,09 × 35,5 – 0,045 × 60) tại sao có cái này vậy bạn? Sao lại lấy khối lượng muối clorua trừ khối lượng muối cacbonat rồi cộng với khối lượng hỗn hợp?

a,b)R + 2HCl---->RCl2+H2(1).
4,8/MR-------------------------4,8/MR.
vì nH2=0,2=>4,8/MR=0,2=>MR=24=>R là Magie (Mg)
c) khối lượng muối =mMgCl2=0.2.MMgCl2=19 gam.
Đổi 400ml=0,4l
nHCl=0,4.1=0,4 (mol)
Gọi Kl hoá trị II là R
Pt: R+2HCl---}RCl2+H2
TheoPt: nR=1/2.nHCl=1/2.0,4=0,2(mol
MR=4,8/0,2=24(g/mol)
R là Al

nH2=2,24/22,4=0,1(mol)
Gọi hóa trị của kim loại R là x(x>0)
PTHH:
2 R+ 2xHCl -> 2RClx+xH2(1)
theo đề bài: 2,4g -> 0.1 mol
theo pt : 2.R -> 0,1x mol
ta có:2,4/2R=0,1/0,1x
-> 0,24x = 0,2R
-> R=12x
Vì lim loại thường có hóa trị 1,2,3
x 1 2 3
R 12 24 36
Kim loại L magie(Mg) L
Vậy kim loại R là Mg
b, n Mg= 2,4/24=0,1 mol
PTHH:Mg+2HCl-> MgCl2+H2 (2)
theo pt(2): nHCl=2nMg=0,2 mol
-> CM của HCl=0,2/0,2=1(M)
lim loại M là kim loại j z bạn
Đổi 200ml=0,2l
nHCl=0,2.2=0,4(mol)
Gọi Kl hoá trị II là R
PTPƯ: R+2HCl----}RCl2+H2
Theo pt:
nR=1/2.nHCl=1/2.0,4=0,2 mol
MR=27,4/0,2=137(g/mol)
R là Bari

Giải thích: Đáp án C
(*) Phương pháp : Bảo toàn khối lượng
- Lời giải :
TQ : CO3 + 2HCl → 2Cl + CO2 + H2O
Mol 0,09 ¬ 0,045 0,045
Bảo toàn khối lượng : mCacbonat + mHCl = mMuối Clorua + mCO2 + mH2O
=> m = 21,495g

Đáp án C
(*) Phương pháp: Bảo toàn khối lượng
-Lời giải:
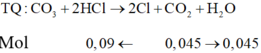
Bảo toàn khối lượng: mCacbonat + mHCl = mMuối Clorua + mCO2 + mH2O
⇒ m = 21 , 495 g

Đáp án D.
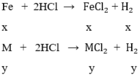
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 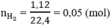
theo bài ra ta có hệ phương trình
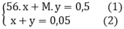
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 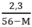
Ta có 0 < y < 0,05
y > 0 ↔ 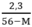 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 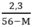 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be
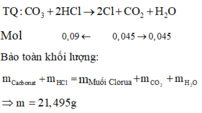
\(PTHH:\) \(XCO_3+2HCl\rightarrow XCl_2+CO_2\uparrow+H_2O\)
\(n_{XCO_3}=\frac{3,94}{X+60}\left(mol\right);n_{CO_2}=\frac{0,448}{22,4}=0,02\left(mol\right)\)
Theo \(PTHH\), \(n_{XCO_3}=n_{CO_2}\)
\(\Rightarrow\frac{3,94}{X+60}=0,02\Rightarrow X=137\left(Ba\right)\)