Cho 200ml dd Al2(SO4)4 1M vào 700ml dd Ba(OH)2 1M. Pư kết thúc thu đc kết tủa. Nung kết tủa tới khối lượng ko đổi thì thu đc m gam chất rắn. Giá trị của m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nhận thấy 3 < nOH- : nAl3+ = 1,4 : 0,4 < 4 → xảy ra quá trình hòa tan kết tủa
Al3+ + 3OH- → Al(OH)3↓
x------3x
Al3+ + 4OH- → Al(OH)4-
y-------4y
Ba2+ + SO42- → BaSO4↓
0,7-----0,6------->0,6
Ta có hệ 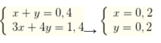
Vậy kết tủa gồm nAl(OH)3 = 0,2 mol, nBaSO4 = 0,6 mol
Nung kết tủa đến khối lượng không đổi: Al2O3: 0,1 mol và nBaSO4 = 0,6 mol → mchất rắn = 150 gam.
Đáp án A

1/ \(n_{KOH}=0,6.0,3=0,18\left(mol\right);n_{AlCl_3}=1,2.0,2=0,24\left(mol\right)\)
\(\Rightarrow n_{OH^-}=0,18\left(mol\right);n_{Al^{3+}}=0,24\left(mol\right)\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
\(0,06\leftarrow0,18\rightarrow0,06\)
\(\Rightarrow m_{Al\left(OH\right)_3}=0,06.78=4,68\left(g\right)\)
2/ \(n_{Al_2\left(SO_4\right)_3}=0,2\left(mol\right);n_{NaOH}=1,75.0,4=0,7\left(mol\right)\)
\(Al_2\left(SO_4\right)_3\rightarrow2Al^{3+}+3SO_4^{2-}\)
\(0,2---\rightarrow0,4---\rightarrow0,6\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
\(0,4--\rightarrow1,2--\rightarrow0,4\)
\(\Rightarrow m_{Al\left(OH\right)_3}=0,4.78=31,2\left(g\right)\)

1.
Các PTPƯ có thể xảy ra theo thứ tự sau:
Gọi số mol Mg và Fe có trong hỗn hợp Q lần lượt là: x và y (mol) Mg + 2AgNO3→ Mg(NO3)2 + 2Ag ↓ (1)
Fe + 2AgNO3→ Fe(NO3)2 + 2Ag ↓ (2)
Fe(NO3)2 + AgNO3→ Fe(NO3)3 + Ag (3)
Theo đề bài ta có: \(\dfrac{6,44}{56}\) = 0,115 < nQ = x + y < \(\dfrac{6,44}{24}\)= 0,2684 (mol)
* Giả sử phản ứng (3) có xảy ra thì chất rắn A chỉ là Ag. Vậy:
nAg > 2x + 2y > 2.0,115 = 0,23 ->mAg > 24,84 > 24,36 (loại)
Vậy: Không xảy ra phản ứng (3). Xét các trường hợp sau:
TH1: Không có (2) suy ra sau (1) dd AgNO3 hết. Chất rắn A gồm Ag, Fe, Mg (có thểdư); dung dịch B chỉ có Mg(NO3)2
Mg(NO3)2→ Mg(OH)2→ MgO. Theo đề 7,0 gam chất rắn là MgO
=> nMgO = nMg(OH)2 = nMg(NO3)2 (l) = 0,175 mol
->nAg(l) = 0,175.2 = 0,35 mol
-> mA > mAg (l) = 0,35 . 108 = 37,8 > 24,36 (loại)
TH2: Có phản ứng (2): Fe pư một phần. (vì nếu Fe hết thì mA>24,84). Gọi số mol Fe phản ứng ở (2) là z mol thì: Chất rắn A thu được gồm: Ag (2x + 2z mol); Fe dư (y - z mol). Dung dịch B gồm: Mg(NO3)2 x mol; Fe(NO3)2 z mol.
Theo đề:
Mg(NO3)2→ Mg(OH)2→ MgO
x → x → x (mol)
Fe(NO3)2 → Fe(OH)2 →+O2; nhiệt độ→ 1/2Fe2O3
z → z → 0,5z (mol)
Vậy ta có hệ phương trình sau:
+ 24x+ 56y = 6, 44
+ 108(2x + 2z) + 56(y+z)=24,36
+ 40x+ 160 . 0,5z = 7
Giải hệ ta đc:
x = 0,035 ; y = 0,1 ; z = 0,07
=> mMg = 0,025 . 24 = 0,84 g ; mFe = 0,1 . 56 = 5,6 g
* Vậy trong Q
%mMg = 0, 84 : 6, 44x100%= 13, 04%; %mFe = 100% - 13, 04% = 86, 96%
* Theo (1), (2) ta có:
nAgNO3 = 2x + 2z = 0,21 mol -> [AgNO3] = p = 0,21 / 0,5 = 0,42M
(gần 1 tiếng của mik đó :( lần sau mấy bài nâng cao này bn nên cho bài chỗ nâng cao ý...cho mấy bác cao trình hơn giải cho :< )


20,4