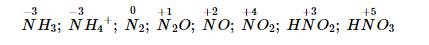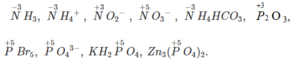Viết cấu trúc Lewis của NO2 và nêu dạng hình học của nó. Dự đoán dạng hình học của ion NO2- và ion NO2+. So sánh hình dạng của 2 ion với NO2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(Fe_2\left(SO_4\right)_3+6KOH->2Fe\left(OH\right)_3\downarrow+3K_2SO_4\)
\(Fe^{3+}+3OH^-->Fe\left(OH\right)_3\)
b) \(Pb\left(NO_3\right)_2+H_2S->PbS\downarrow+2HNO_3\)
\(Pb^{2+}+S^{2-}->PbS\)
c) \(Fe+6HNO_3-->Fe\left(NO_3\right)_3+3NO_2+3H_2O\)
\(Fe+6H^++3NO_3^-->Fe^{3+}+3NO_2+3H_2O\)

a) H2SO3
Gọi x là số oxi hóa của S, theo quy tắc 1 và 2 có:
2.(+1) + 1.x + 3.(-2) = 0 → x = +4.
Vậy số oxi hóa của H là +1, của S là +4, của O là -2.
b) Al(OH)4-
Gọi x là số oxi hóa của Al, theo quy tắc 1 và 2 có:
1.x + 4.[1.(-2) + 1.(+1)] = -1 → x = +3.
Vậy số oxi hóa của Al là +3, của O là -2, của H là +1.
c) NaAlH4
Gọi x là số oxi hóa của H, theo quy tắc 1 và 2 có:
1.(+1) + 1.(+3) + 4.x = 0 → x = -1.
Vậy số oxi hóa của Na là +1, của Al là +3, của H là -1.
d) NO2-
Gọi x là số oxi hóa của N, theo quy tắc 1 và 2 có:
1x + 2.(-2) = -1 → x = +3.
Vậy số oxi hóa của N là +3, của O là -2