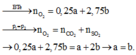Trộn 3 MOL SO2 với 2 MOL O2. Cho hỗn hợp vào bình kín chứa phản chất xúc tác V2O5, bật tia lửa điện để phản ứng xảy ra . Sau phản ứng đưa bình về điệu kiện ban đầu thì thấy áp suất trong bình giảm 10%. Tính hiệu suất của phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C.
Gọi x là số mol oxi đã phản ứng, ta có:
Tổng số mol khí trước phản ứng là: 3 + 2 = 5 mol
Tổng số mol khí sau phản ứng là: 5 – x
![]()
Xét tỉ lệ giữa số mol và hệ số cân bằng của SO2 và O2, SO2 hết, O2 dư
![]()

Đáp án : B
SO2 + 0,5O2 -> SO3
H tính theo SO2 => nSO3 = 0,1.0,8 = 0,08 mol = nBaSO4
=> mBaSO4 = 18,64g ( SO2 không phản ứng với BaCl2)

1)
Xét tỉ lệ: \(\dfrac{3}{2}< \dfrac{2}{1}\) => Hiệu suất tính theo SO2
\(n_{SO_2\left(pư\right)}=\dfrac{3.75}{100}=2,25\left(mol\right)\)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
2,25--------------------->2,25
=> nSO3 = 2,25 (mol)
2) Gọi số mol SO2 pư là a (mol)
PTHH: 2SO2 + O2 -----V2O5,to-----> 2SO3
Trc pư: 3 2 0
Pư: a-->0,5a-------------------->a
Sau pư: (3-a) (2-0,5a) a
=> (3-a) + (2-0,5a) + a = 4,25
=> a = 1,5 (mol)
=> \(H=\dfrac{1,5}{3}.100\%=50\%\)