Có hỗn hợp khí CO và CO2. Nếu cho hỗn hợp này tác dụng với dung dịch Ca(OH)2 dư sinh ra 15 gam kết tủa trắng. Nếu cho hỗn hợp này tác dụng với Fe2O3 dư thu được 11,2 gam kim loại. Xác định % theo thể tích hỗn hợp khí ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Xác định thành phần của hỗn hợp khí :
- Số mol CO 2 có trong hỗn hợp được tính theo (1) :
n CO 2 = n CaCO 3 = 1/100 = 0,01 mol
- Số mol CO có trong hỗn hợp được tính theo (2) :
n CO = n Cu = 0,64/64 = 0,01
Thành phần phần trăm theo thể tích của hỗn hợp khí được tính theo số mol của mỗi khí. Ta có kết quả : Hỗn hợp khí có 50% thể tích của mỗi khí.

Các phương trình hoá học :
- CO 2 tác dụng với dung dịch Ca OH 2 dư, sinh ra kết tủa CaCO 3 :
CO 2 + Ca OH 2 → CaCO 3 ↓+ H 2 O (1)
- CO khử CuO thành kim loại Cu màu đỏ :
CO + CuO → CO 2 + Cu (2)

Hỗn hợp khí B gồm CO và CO2 khi tác dụng với dd chứa 0,025 mol Ca(OH)2 chắc chắc tạo 2 muối
Ta có: \(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,02______0,02______0,02 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
0,01_____0,005_______0,005 (mol)
\(\Rightarrow n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO_2}=0,03\cdot44=1,32\left(g\right)\)
Bảo toàn nguyên tố: \(n_{CO\left(p/ứ\right)}=n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO}=0,03\cdot28=0,84\left(g\right)\)
Bảo toàn khối lượng: \(m_A=m_{oxit}+m_{CO}-m_{CO_2}=1,12\left(g\right)\)
PTHH: \(2A+2zHCl\rightarrow ACl_z+zH_2\uparrow\) (z là hóa trị của A)
Ta có: \(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_A=\dfrac{0,04}{z}\left(mol\right)\) \(\Rightarrow M_A=\dfrac{1,12}{\dfrac{0,04}{z}}=28z\)
Ta thấy với \(z=2\) thì \(M_A=56\) \(\Rightarrow\) Kim loại A là Fe
Gọi công thức oxit cần tìm là FexOy
Bảo toàn Oxi: \(n_{O\left(oxit\right)}=2n_{CO_2}-n_{CO}=0,03\left(mol\right)\)
Xét tỉ lệ \(x:y=0,02:0,03=2:3\)
Vậy công thức oxit là Fe2O3

Đáp án D
Sơ đồ quá trình phản ứng
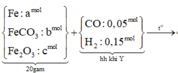
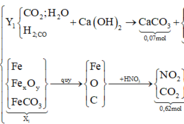

Hướng tư duy 1:
+ Xét khí Y1 có ![]()
![]()
+Xét hỗn hợp X1(sau khi quy đổi) có:
![]()
![]()
Do đó, trong 0,62 mol hỗn hợp khí có (0,67-b) mol NO (khí hóa nâu)
Bảo toàn nguyên tố Fe có:
![]()
= a + b = 2c mol
Bảo toàn O: ![]()
![]()
![]()
Bảo toàn e:
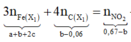
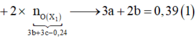
+ Xét hỗn hợp khí sau khi tác dụng H 2 S O 4 ta có:
![]()
![]()
Mà ![]()
=> giải hệ (1), (2), (3) ta được
![]()
Hướng tư duy 2:
Gọi x là số mol F e C O 3 bị nhiệt phân
Bảo toàn C ta có: ![]() = 0,05 mol
= 0,05 mol
=>
n
C
O
(
p
h
ả
n
ứ
n
g
)
= ![]()
![]()
+ Gọi a là số mol
F
e
C
O
3
phản ứng với
H
N
O
3
có ngay ![]()
+ Cho X phản ứng với H 2 S O 4 (đặc, nóng): (X chứa a+0,05 mol F e C O 3 )
Bảo toàn nguyên tố C có: ![]()
![]()
Bảo toàn e trong phản ứng với H N O 3 và H 2 S O 4 đặc nóng, có hệ:
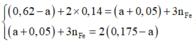
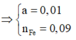
![]()
![]()
