Dùng khí H2 để khử 24g hỗn hợp Fe2O3 và CuOói khối lượng CuO chiếm gần 33,34%. Khối lượng Fe Và Cu thu được sau phản ứng là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=20-8=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1--->0,1------>0,1
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,075--->0,225----->0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mFe = 0,15.56 = 8,4 (g)
b) \(V_{H_2}=\left(0,1+0,225\right).22,4=7,28\left(l\right)\)

\(n_{Fe_2O_3}=24.75\%=18g\)
\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(n_{CuO}=\dfrac{24-18}{80}=0,075mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1125 0,3375 ( mol )
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,075 0,075 ( mol )
\(V_{H_2}=\left(0,3375+0,075\right).22,4=9,24l\)

\(m_{Fe_2O_3}=16\cdot75\%=12\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{12}{160}=0.075\left(mol\right)\)
\(n_{CuO}=16\cdot25\%=4\left(g\right)\)
\(n_{CuO}=\dfrac{4}{80}=0.05\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(n_{H_2}=3\cdot0.075+0.05=0.275\left(mol\right)\)
a,\(m_{Fe_2O_3}=16.75\%=12\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
\(m_{CuO}=16-12=4\left(g\right)\Rightarrow n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,075 0,225 0,15
PTHH: CuO + H2 → Cu + H2O
Mol: 0,05 0,05 0,05
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right);m_{Cu}=0,05.64=3,2\left(g\right)\)
b,\(n_{H_2}=0,225+0,05=0,275\left(mol\right)\)

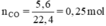
Áp dụng định luật bảo toàn khối lượng ta có :
30 + mCO = m + mCO2 → m = 30 + 0,25 x 28 – 0,25 x 44 = 26 (g)
Đáp án B.

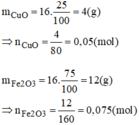
PTHH của phản ứng là:
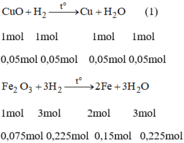
Từ pt (1), ta có: n C u = n C u O = 0,05 mol
m C u = 0,05.64 = 3,2(g)
Từ pt (2), ta có n F e = 2 . n F e 2 O 3 = 2. 0,075 = 0,15 mol
m F e = 0,15.56 = 8,4(g)

\(a) CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ b) n_{CuO} = \dfrac{32.25\%}{80} = 0,1(mol)\\ n_{Fe_2O_3} = \dfrac{32-0,1.80}{160} = 0,15(mol)\\ n_{Cu} = n_{CuO} = 0,1(mol) \Rightarrow m_{Cu} = 0,1.64 = 6,4(gam)\\ n_{Fe} = 2n_{Fe_2O_3} = 0,3(mol) \Rightarrow m_{Fe} = 0,3.56 = 16,8(gam)\)

a, mFe2O3 = 32 . 75% = 24 (g)
nFe2O3 = 24/160 = 0,15 (mol)
mCuO = 32 - 24 = 8 (g)
nCuO = 8/80 = 0,1 (mol)
PTHH:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
0,15 ---> 0,45 ---> 0,3
CuO + H2 -> (t°) Cu + H2O
0,1 ---> 0,1 ---> 0,1
mFe = 0,3 . 56 = 16,8 (g)
mCu = 64 . 0,1 = 6,4 (g)
b, nH2 = 0,1 + 0,45 = 0,55 (mol)
VH2 = 0,55 . 22,4 = 12,32 (l)
c, PTHH:
2Al + 6HCl -> 2AlCl3 + 3H2
11/30 <--- 1,1 <--- 11/30 <--- 0,55
mAl = 11/30 . 27 = 9,9 (g)
mHCl = 1,1 . 36,5 = 40,15 (g)

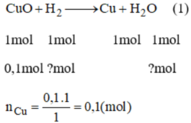
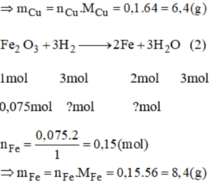
Ta có:
\(\left\{{}\begin{matrix}m_{CuO}=\frac{24.33,34}{100}=8\left(g\right)\\n_{Cu}=\frac{8}{80}=0,1\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Fe2O3}=24-8=16\left(g\right)\\n_{Fe2O3}=\frac{16}{160}=0,1\left(mol\right)\end{matrix}\right.\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,1_____________0,1_________
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,1____________0,2____________
\(\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
Cảm ơn bạn á