Cho 1,38 gam KL kiềm tác dụng với H2O dư thu được 0,672 lit H2 (đktc). Xác định tên KL
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2X + 2nH2O → 2XOHn + nH2
Mol: \(\dfrac{0,5}{n}\) 0,25
\(\Rightarrow M_X=\dfrac{10}{\dfrac{0,5}{n}}=20n\left(g/mol\right)\)
Vì X là kim loại nên có hóa trị l,ll,lll
| n | l | ll | lll |
| Mx | 20 | 40 | 60 |
| Kết luận | loại | thỏa mãn | loại |
⇒ X là canxi (Ca)

Gọi 2 kim loại kiềm của nhóm IA là M
n h2 = 0,224: 22,4=0,01 mol
M + 2H2O -> 2MOH + H2
n M = 0,3/ M M = n H2 = 0,01
=> M M = 30 đvc
mà M là 2 kim loại kiềm thuộc chu kì liên tiếp
=> M gồm Li và Na
xin lỗi mk làm nhầm
gọi 2 kl kiềm của nhóm IA là R
n H2 = 0,224:22,4=0,01 mol
n R = 0,3/ M R mol
2R + 2H2O -> 2ROH +H2
=> nR = n H2 .2
=> 0,3/M R = 0,02
=> M R =15 đvc
ko có gt nào tm

Gọi kim loại kiềm là R.
PTHH: 2R + 2xH2O ---> 2R(OH)x + xH2
Ta có: \(n_{H_2}=\dfrac{0,48}{2}=0,24\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{x}.n_{H_2}=\dfrac{2}{x}.0,24=\dfrac{0,48}{x}\left(mol\right)\)
=> \(M_R=\dfrac{11,04}{\dfrac{0,48}{x}}=\dfrac{11,04x}{0,48}=23x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 |
| M | 23 | 46 | 69 |
| Na | loại | loại |
Vậy kim loại kiềm là natri (Na)

\(KL:A\left(II\right)\\ n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ A+2H_2O\rightarrow A\left(OH\right)_2+H_2\\ n_A=n_{AOH}=n_{H_2}=0,25\left(mol\right)\\ \Rightarrow M_A=\dfrac{10}{0,25}=40\left(\dfrac{g}{mol}\right)\\ \Rightarrow A\left(II\right):Canxi\left(Ca=40\right)\\ m_{Ca\left(OH\right)_2}=74.0,25=18,5\left(g\right)\\ m_{ddCa\left(OH\right)_2}=10+200-0,25.2=209,5\left(g\right)\\ C\%_{ddCa\left(OH\right)_2}=\dfrac{18,5}{209,5}.100\approx8,831\%\)

\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(M+2H_2O\rightarrow M\left(OH\right)_2+H_2\)
\(0.2........................................0.2\)
\(M_M=\dfrac{8}{0.2}=40\left(\dfrac{g}{mol}\right)\)
\(M:Ca\left(Canxi\right)\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
_____0,2<--------------------------0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)=>Ca\)

Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 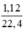 = 0,05(mol)
= 0,05(mol)
PTHH: 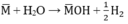
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 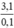 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
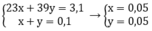
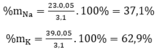

Bạn xem lại đề nhé, nếu 11,7g kim loại thì không có kim loại thỏa mãn nhé, nesu 1,17g thì tìm đc kim loại K(kali).
Gọi kim loại kiềm là R
PTHH: 2R + 2xH2O ---> 2R(OH)x + xH2
Ta có: \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{x}.n_{H_2}=\dfrac{2}{x}.0,03=\dfrac{0,06}{x}\left(mol\right)\)
=> \(M_R=\dfrac{1,38}{\dfrac{0,06}{x}}=\dfrac{1,38x}{0,06}=23x\left(g\right)\)
Biện luận:
Vậy kim loại kiềm là natri (Na)
Gọi kim loại kiềm cần tìm là M. (kim loại kiềm có hóa trị l)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)
\(2M+H_2O\rightarrow M_2O+H_2\)
0,06 0,03
\(\Rightarrow n_M=\dfrac{1,38}{\overline{M_M}}=0,06\) \(\Rightarrow\overline{M_M}=23\left(Na\right)\)
Vậy kim loại M cần tìm là Natri(Na).