Ta thu được khối lượng muối bao nhiêu nếu cho 2,24 lít khí H2S vào 150ml dung dịch NaOH 1M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,15.1=0,15\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0,15}{0,1}=1,5\)
=> Tạo ra 2 muối Na2S, NaHS
PTHH: 2NaOH + H2S --> Na2S + 2H2O
a------>0,5a---->0,5a
NaOH + H2S --> NaHS + H2O
b----->b-------->b
=> \(\left\{{}\begin{matrix}a+b=0,15\\0,5a+b=0,1\end{matrix}\right.\)
=> a = 0,1 (mol); b = 0,05 (mol)
=> \(\left\{{}\begin{matrix}m_{Na_2S}=0,05.78=3,9\left(g\right)\\m_{NaHS}=0,05.56=2,8\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}C_{M\left(Na_2S\right)}=\dfrac{0,05}{0,15}=0,33M\\C_{M\left(NaHS\right)}=\dfrac{0,05}{0,15}=0,33M\end{matrix}\right.\)

Chọn C
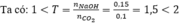
Vậy sau phản ứng thu được 2 muối: NaHCO 3 (x mol) và Na 2 CO 3 (y mol)
Bảo toàn Na có: x + 2y = 0,15 (1)
Bảo toàn C có: x + y = 0,1 (2)
Từ (1) và (2) có x = y = 0,05.
Khối lượng muối có trong Y là m = 0,05 (84 + 106) = 9,5 gam.

\(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,1---->0,1
=> mNa2S = 0,1.78 = 7,8 (g)

9
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g) =>D
10
nBa(OH) = 0,15.1 = 0,15mol; nBaCO3 = 19,7 : 197 = 0,1mol
Vì nBaCO3 < nBa(OH)2 → xét 2 trường hợp
Trường hợp 1: Ba(OH)2 dư, CO2 hết, phản ứng chỉ tạo muối cacbonat
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
Vậy V = VCO2 = 0,1.22,4 =2,24
Trường hợp 2: Phản ứng sinh ra 2 muối cacbonat và hiđrocacbonat
CO2 + Ba(OH)2→ BaCO3 + H2O (1)
0,1 0,1 0,1
2CO2+Ba(OH)2→Ba(HCO3)2
0,1 0,05
Theo phương trình (1): nBa(OH)2(1) = nBaCO3=0,1mol
Mà nBa(OH)2= 0,15mol →nBa(OH)2 (2) = 0,15−0,1 = 0,05mol
Theo (1) và (2): nCO2 = nBaCO3 + 2nBa(OH)2 (2) = 0,1 + 2.0,05 = 0,2 mol
Vậy V = VCO2 = 0,2.22,4 = 4,48 lít
=>A

nKOH = 0,15 . 2 = 0,3 (mol)
nH2S = 2,24/22,4 = 0,1 (mol)
PTHH: 2KOH + H2S -> K2S + 2H2O
LTL: 0,3/2 > 0,1 => KOH dư
nKOH (p/ư) = 0,1 . 2 = 0,2 (mol)
nKOH (dư) = 0,3 - 0,2 = 0,1 (mol)
nK2S = 0,1 (mol)
CMK2S = 0,1/0,15 = 0,66M
CMKOH = 0,1/0,15 = 0,66M

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,4.0,4=0,16\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,16}{0,1}=1,6\)
=> Tạo ra muối Na2CO3 và NaHCO3
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
0,16--->0,08---->0,08
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,02<---0,02------------->0,04
=> \(\left\{{}\begin{matrix}m_{Na_2CO_3}=\left(0,08-0,02\right).106=6,36\left(g\right)\\m_{NaHCO_3}=0,04.84=3,36\left(g\right)\end{matrix}\right.\)
=> mmuối = 6,36 + 3,36 = 9,72 (g)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{NaOH}=0,4.0,4=0,16\left(mol\right)\)
\(T=\dfrac{0,16}{0,1}=1,6\rightarrow\) Tạo cả 2 muối
Gọi \(\left\{{}\begin{matrix}n_{Na_2CO_3}=a\left(mol\right)\\n_{NaHCO_3}=b\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + CO2 ---> Na2CO3 + H2O
2a a a
NaOH + CO2 ---> NaHCO3
b b b
Hệ pt: \(\left\{{}\begin{matrix}2a+b=0,16\\a+b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,06\left(mol\right)\\b=0,04\left(mol\right)\end{matrix}\right.\)
=> mmuối = 0,06.106 + 0,04.84 = 9,72 (g)

Bạn tính số mol của \(H_2S\) và \(NaOH\) ( hoặc là \(KOH\) ) sau đó so sánh tỉ lệ như sau:
\(\frac{n_{OH}}{n_{H_2S}}< 1\rightarrow NaHS\) ( Chỉ tạo ra muối NaHS)
\(\frac{n_{OH}}{n_{H_2S}}>2\rightarrow Na_2S\) ( Chỉ tạo ra muối Na2S)
\(1< \frac{n_{OH}}{n_{H_2S}}< 2\rightarrow NaHS+Na_2S\) ( Tạo ra hỗn hợp 2 muối)
- Lưu ý với bài trên:
+ Đổi cm3 ra l
+ Nếu tạo hh 2 muối thì viết 2 PTHH và đặt ẩn

\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(T=\dfrac{0.2}{0.1}=2\)
=> Tạo muối trung hòa
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(0.2...........0.1.................0.1\)
\(m_{Na_2CO_3}=0.1\cdot106=10.6\left(g\right)\)
Không tính được nồng độ mol nhé !
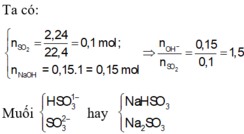
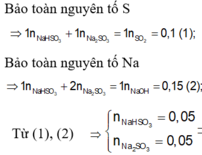
Ta có:
\(n_{H2S}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,15.1=0,15\left(mol\right)\)
\(\Rightarrow\frac{n_{NaOH}}{n_{H2S}}=\frac{0,15}{0,1}=1,5\)
Vì 1 <1,5<2 nên sản phẩm tạo ra 2 muối.
\(NaOH+H_2S\rightarrow NaHS+H_2O\)
\(2NaOH+H_2S\rightarrow Na_2S+2H_2O\)
Gọi số mol NaHS; Na2S lần lượt là x, y.
\(\Rightarrow\left\{{}\begin{matrix}n_{NaOH}=x+2y=0,15\\n_{H2S}=x+y=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\Rightarrow m_{NaHS}=0,05.\left(23+1+32\right)=2,8\left(g\right)\)
\(m_{Na2S}=0,05.\left(23.2+32\right)=3,9\left(g\right)\)