Hỗn hợp B gồm Zn, Fe và Cu được chia làm hai phần bằng nhau. Phần thứ nhất cho phản ứng với dung dịch H2SO4 đặc, nóng, dư thu được 2,24 lít khí SO2 (đktc). Phần thứ hai cho phản ứng vừa đủ với bột lưu huỳnh nung nóng trong điều kiện không có oxi, thu được 7,38 gam hỗn hợp rắn C. Cho C phản ứng với dung dịch H2SO4 loãng dư thu được khí D. Toàn bộ khí D phản ứng vừa đủ với 0,6 lít dung dịch CuSO4 0,1M. Biết các phản ứng xảy ra hoàn toàn. Tính khối lượng mỗi kim loại trong B
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

19 tháng 8 2018
Đáp án : C
P1 : nH2 = nFe = 0,1 mol
P2 : Gọi số mol của Fe và Cu trong P2 lần lượt là x và y
=> bảo toàn e : 3x + 2y = 2nSO2 = 0,8 mol
, mmuối = mCuSO4 + mFe2(SO4)3 = 200x + 160y = 56g
=> x = 0,2 ; y = 0,1 mol
Tỉ lệ mol Fe : Cu trong các phần không đổi
=>Trong P1 : nCu = 0,05 mol
Trong m gam X có: 0,3 mol Fe và 0,15 mol Cu
=> m = 26,4g





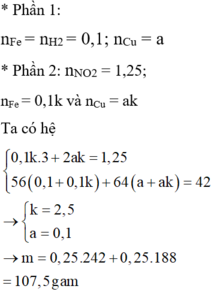
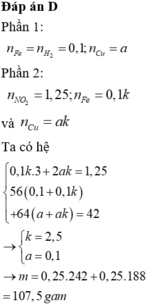
Mỗi phần có a, b, c mol Zn , Fe , Cu
Phần 1 :
\(n_{SO2}=0,1\left(mol\right)\)
Bảo toàn e : \(2a+3b+2c=0,1.2=0,2\left(2\right)\)
Phần 2 :
Bảo toàn nguyên tố :
\(n_{ZnS}=n_{Zn}=a\)
\(n_{FeS}=n_{Fe}=b\)
\(n_{CuS}=n_{Cu}=c\)
\(\Rightarrow97a+88b+96c=7,38\left(2\right)\)
\(CuSO_4+H_2S\rightarrow CuS+H_2SO_4\)
0,06_______0,06_________________
\(n_{H2S}=n_{ZnS}+n_{FeS}\left(BT:S\right)\) Vì CuS không tan trong H2SO4
\(\Rightarrow a+b=0,06\left(3\right)\)
\(\left(1\right)+\left(2\right)+\left(3\right)\Rightarrow\left\{{}\begin{matrix}a=0,02\\b=0,04\\c=0,02\end{matrix}\right.\)
B có 2a , 2b ,2c mol Zn, Fe, Cu
\(\Rightarrow m_{Zn}=65.2a=2,6\left(g\right)\)
\(\Rightarrow m_{Fe}=56.2b=4,48\left(g\right)\)
\(\Rightarrow m_{Cu}=64.2c=2,52\left(g\right)\)